题目内容
16.原子间通过共用电子对形成的相互作用叫做共价键.成键微粒是原子,由共价键形成的化合物叫共价化合物.共价化合物一般包括非金属氢化物如H2O,非金属氧化物如CO2,含氧酸如H2SO4,个别盐如AlCl 3和大部分有机化合物如乙醇等.分析 共价键是原子之间通过共用电子对形成的,由共价键形成的化合物是共价化合物,非金属氢化物、非金属氧化物、含氧酸等属于共价化合物.
解答 解:非金属原子间,不容易得失电子,原子间通过共用电子对形成的相互作用叫共价键,由共价键形成的化合物是共价化合物,非金属氢化物如H2O、非金属氧化物如CO2、含氧酸H2SO4等属于共价化合物.
故答案为:通过共用电子对形成的相互作用;原子;共价键;H2O;CO2;H2SO4.
点评 本题考查了化学键的概念,明确物质的构成微粒及微粒间作用力即可判断化学键,注意化学键概念中的几个关键词“相邻”、“强烈”、“相互作用”,为易错点,题目难度不大.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
6.NA为阿佛加德罗常数,下列叙述正确的是( )
| A. | 17 g NH3所含氢原子数目为3NA | |
| B. | 1L 1mol/L的盐酸溶液中,含氯化氢分子数为NA | |
| C. | 标准状况下,11.2L四氯化碳所含分子数为0.5 NA | |
| D. | 在同温同压时,相同体积的任何气体单质所含的原子数相同 |
7.下列说法中正确的是( )
| A. | 1molS的质量是32g/mol | B. | 27g铝的物质的量为1 | ||
| C. | CO的摩尔质量为28g/mol | D. | 2H2O的摩尔质量为18g/mol |
11.A、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它所处的同族中最小的.试确定:
(1)写出下列各元素的名称:(注意:写元素符号)
A:硅,B:氮,C:硫,D:砷.
(2)C、D、X最高价氧化物对应水化物酸性由强到弱的顺序:(填化学式)H2SO4>H3PO4>H3ASO4
(3)写出A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序:NH3>PH3>SiH4.
(4)下列关于D元素化合物的性质叙述中不正确的是C
A.D的单质在通常状况下是固体
B.D难以与H2化合生成氢化物
C.气态氢化物有两种,为DH3和DH5.
| B | ||
| A | X | C |
| D |
A:硅,B:氮,C:硫,D:砷.
(2)C、D、X最高价氧化物对应水化物酸性由强到弱的顺序:(填化学式)H2SO4>H3PO4>H3ASO4
(3)写出A、B、X气态氢化物的化学式,并排列稳定性由强到弱的顺序:NH3>PH3>SiH4.
(4)下列关于D元素化合物的性质叙述中不正确的是C
A.D的单质在通常状况下是固体
B.D难以与H2化合生成氢化物
C.气态氢化物有两种,为DH3和DH5.
1.下列反应过程中,最终溶液保持原来颜色的是( )
| A. | 向滴有酚酞的NaOH溶液中通入过量的CO2气体 | |
| B. | 向酸性KMnO4溶液中加入足量的H2O2 | |
| C. | 向含有KSCN的FeC13溶液中加入足量的Cu粉 | |
| D. | 向品红溶液中通入足量的等体积混合的Cl2与SO2气体 |
5.关于常温下pH=12的NaOH溶液,下列说法正确的是( )
| A. | c(OH-)>c(Na+)+c(H+) | |
| B. | 由水电离出的c(OH-)=1.0×10-2mol﹒L-1 | |
| C. | 与等体积pH=2的醋酸混合后所得溶液显碱性 | |
| D. | 与等体积0.01mol﹒L-1氯化铵溶液混合后所得溶液中:c(Na+)=c(Cl-) |
6.Fe3+和I-在水溶液中反应如下:2I-+2Fe3+?2Fe2++I2(水溶液).
(1)当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,化学反应速率减慢(填“增大”“减慢”或“不变”),v(正)>v(逆)填“>”“<”或“=”).
(2)该反应的正反应速率和Fe3+、I-的浓度关系为v=kcm(I-)•cn(Fe3+)(k为常数).
通过所给的数据计算得知:在v=kcm(I-)•cn (Fe3+)中,m、n的值为C
A.m=1、n=1 B.m=1、n=2 C.m=2、n=1 D.m=2、n=2
I-浓度对反应速率的影响大于(填“>”“<”或“=”)Fe3+浓度对反应速率的影响.
(1)当上述反应达到平衡后,加入CCl4萃取I2,且温度不变,化学反应速率减慢(填“增大”“减慢”或“不变”),v(正)>v(逆)填“>”“<”或“=”).
(2)该反应的正反应速率和Fe3+、I-的浓度关系为v=kcm(I-)•cn(Fe3+)(k为常数).
| c(I-)/mol•L-1 | c(Fe3+)/mol•L-1 | v/mol•L-1•s-1 | |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |
A.m=1、n=1 B.m=1、n=2 C.m=2、n=1 D.m=2、n=2
I-浓度对反应速率的影响大于(填“>”“<”或“=”)Fe3+浓度对反应速率的影响.
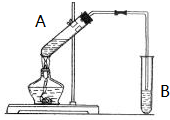 实验室用如图所示的装置制取乙酸乙酯.
实验室用如图所示的装置制取乙酸乙酯. CH3COOC2H5+H2O.
CH3COOC2H5+H2O.