题目内容
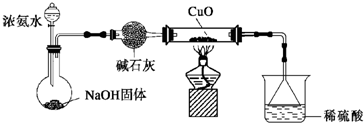
19.某天然产的无色晶体,硬度仅次于金刚石,因此它常被用来制造砂轮,用以加工光学仪器.该无色晶体由两种短周期元素组成,其中A元素的正三价阳离子与氖原子的电子层结构相同;B元素原子的最外层电子数是其电子层数的三倍.根据以上叙述,请回答:(1)A元素原子的原子结构示意图为
 .
.(2)A元素在周期表中的位置为三周期ⅢA族,B元素的名称是氧.
(3)最高正化合价的碳元素与B元素组成的化合物的化学式为CO2,其化学键的类型为共价 键(填“离子”或“共价”).
(4)A元素的简单阳离子与B元素的简单阴离子的半径比值小于1(填“大于”或“小于”)
(5)A元素的最高价氧化物对应水化物的一种用途是治疗胃酸过多等,其与氢氧化钠溶液反应的化学方程式是:Al(OH)3+NaOH→NaAlO2+2H2O.
分析 A元素的正三价阳离子与氖原子的电子层结构相同,即A原子失去将个电子后与氖原子相同,氖为10号元素,所以应为13号元素,即A为Al,B元素原子的最外层电子数是其电子层数的三倍,B至少有两个电子层,若为两个电子层,则B最外层电子数为6,所以B为O,若有3个电子层,则B最外层有9个电子,不符合实际,故B为O,据此答题.
解答 解:A元素的正三价阳离子与氖原子的电子层结构相同,即A原子失去将个电子后与氖原子相同,氖为10号元素,所以应为13号元素,即A为Al,B元素原子的最外层电子数是其电子层数的三倍,B至少有两个电子层,若为两个电子层,则B最外层电子数为6,所以B为O,若有3个电子层,则B最外层有9个电子,不符合实际,故B为O,
(1)铝的原子结构示意图为  ,
,
故答案为: ;
;
(2)铝元素在周期表中的位置为第三周期第ⅢA族,B为O,B元素的名称是氧,
故答案为:三;ⅢA;氧;
(3)B为O,最高正化合价的碳元素与B元素组成的化合物的化学式为CO2,其化学键的类型为共价键,
故答案为:CO2;共价;
(4)核外电子层数相同时,核电荷数越多,离子半径越小,Al元素的简单阳离子与O元素的简单阴离子的半径比值小于1,
故答案为:小于;
(5)氧化铝可以用来治疗胃酸过多等,其与氢氧化钠溶液反应的化学方程式是Al(OH)3+NaOH→NaAlO2+2H2O,
故答案为:治疗胃酸过多等;Al(OH)3+NaOH→NaAlO2+2H2O;
点评 本题考查原子结构与元素周期律的性质,题目难度中等,本题注意把握原子的结构特点,为解答该题的关键,注意元素周期律的应用和化学用语的正确书写.

练习册系列答案
相关题目
9.工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)?Si(s)+4HCl(g);△H=+QkJ/mol(Q>0)某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是( )
| A. | 反应过程中,若增大压强能提高SiCl4的转化率 | |
| B. | 若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ | |
| C. | 在温度、体积不变的情况下,若按照起始充入比例再向容器中充入反应物,重新达平衡后,HCl的体积分数不变 | |
| D. | 当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好反应 |
10.下列有关化学实验基本知识和基本操作的描述不正确的是( )
| A. | 丁达尔效应可以用于区别FeCl3溶液和Fe(OH)3胶体 | |
| B. | 过滤和蒸发操作均用到玻璃棒,但玻璃棒的作用不相同 | |
| C. | 加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有CO32- | |
| D. | 氨气能使湿润的红色石蕊试纸变蓝,说明氨气的水溶液呈碱性 |
14.现有甲、乙、丙三种元素,其原子序数都不超过20.有关信息如下:
下列关于甲、乙、丙三种元素相关的分析正确的是( )
| 元素代号 | 相关信息 |
| 甲 | n为电子层数,甲原子最外层电子数为(2n2-1) |
| 乙 | 在周期表中它的周期数为k,主族序数为(2k+1) |
| 丙 | 电子层数大于最外层电子数 |
| A. | 甲的单质难溶于水 | |
| B. | 乙的气态氢化物遇湿润的pH试纸变红色或蓝色 | |
| C. | 丙的最高价氧化物对应的水化物是强碱 | |
| D. | 甲、丙只能形成共价化合物 |
10.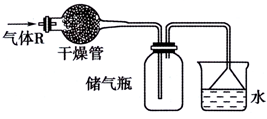 实验室里可按如图所示的装置干燥、储存气体R,多余的气体可用水吸收,则R是( )
实验室里可按如图所示的装置干燥、储存气体R,多余的气体可用水吸收,则R是( )
 实验室里可按如图所示的装置干燥、储存气体R,多余的气体可用水吸收,则R是( )
实验室里可按如图所示的装置干燥、储存气体R,多余的气体可用水吸收,则R是( )| A. | NO | B. | HCl | C. | O2 | D. | NH3 |
7.下列有关能量转换的说法正确的是( )
| A. | 铅蓄电池的放电过程是电能转化为化学能 | |
| B. | 化石燃料和植物燃料燃烧时放出的能量是化学能转化为光能 | |
| C. | 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程 | |
| D. | 植物通过光合作用将CO2转化为葡萄糖是太阳能大部分转变成化学能的过程 |
8. A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.
A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.
(1)在标准状况下为液体的卤素单质是C (填字母,下同),为固体的卤素单质是D.
(2)A的相对分子质量为38(保留整数)
(3)写出B与水反应的化学方程式Cl2+H2O=HCl+HClO
(4)卤素单质B、C、D的氧化性由大到小的顺序为Cl2>Br2>I2(用化学式表示)
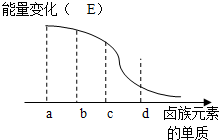
(5 )卤族元素的单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示卤族中某一元素的单质,E为相同物质的量的单质与H2反应过程中的能量变化(△E越大,表明反应越容易发生).请回答下列问题:d为I2(写化学式,下同),红热的铜丝在b单质中燃烧的现象为剧烈燃烧,产生棕黄色的烟..
 A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.
A、B、C、D为按顺序排列的前四种卤素单质,仔细分析下表中的数据,回答有关问题.| 卤素单质 | 密度(标准状况下) | 沸点/℃ | 熔点/℃ | 溶解度(标准状况下,100g水中) |
| A | 1.696 g•l-1 | -188.1 | -219.6 | -- |
| B | 3.214 g•l-1 | -34.6 | -101 | 226 cm3 |
| C | 3.119 g•cm-3 | 58.78 | -7.2 | 4.16 g |
| D | 4.93 g•cm-3 | 184.4 | 113.5 | 0.029 g |
(2)A的相对分子质量为38(保留整数)
(3)写出B与水反应的化学方程式Cl2+H2O=HCl+HClO
(4)卤素单质B、C、D的氧化性由大到小的顺序为Cl2>Br2>I2(用化学式表示)
(5 )卤族元素的单质与H2反应过程中的能量变化如图所示,其中a、b、c、d分别表示卤族中某一元素的单质,E为相同物质的量的单质与H2反应过程中的能量变化(△E越大,表明反应越容易发生).请回答下列问题:d为I2(写化学式,下同),红热的铜丝在b单质中燃烧的现象为剧烈燃烧,产生棕黄色的烟..