题目内容
白酒、食醋、蔗糖、淀粉是家庭厨房中常用的烹调剂,利用这些物质能完成的实验是( )
| A、鉴别食盐和小苏打 |
| B、检验食盐中是否含KIO3 |
| C、检验自来水中是否含有氯离子 |
| D、检验白酒中是否含甲醇 |
考点:物质的检验和鉴别的基本方法选择及应用
专题:物质检验鉴别题
分析:A.小苏打与食醋反应生成气体,而氯化钠不能;
B.淀粉遇碘单质变蓝,不能得到碘单质;
C.检验氯离子,需要硝酸和硝酸银;
D.鉴别乙醇和甲醇可以用碘仿反应,需要碘单质、NaOH.
B.淀粉遇碘单质变蓝,不能得到碘单质;
C.检验氯离子,需要硝酸和硝酸银;
D.鉴别乙醇和甲醇可以用碘仿反应,需要碘单质、NaOH.
解答:
解:A.小苏打与食醋反应生成气体,而氯化钠不能,则利用食醋可鉴别,故A正确;
B.淀粉遇碘单质变蓝,食盐中含KIO3,不能得到碘单质,则不能检验,还需要KI,故B错误;
C.检验氯离子,需要硝酸和硝酸银,缺少试剂,不能完成,故C错误;
D.鉴别乙醇和甲醇可以用碘仿反应,需要碘单质、NaOH,缺少试剂,不能完成,故D错误;
故选A.
B.淀粉遇碘单质变蓝,食盐中含KIO3,不能得到碘单质,则不能检验,还需要KI,故B错误;
C.检验氯离子,需要硝酸和硝酸银,缺少试剂,不能完成,故C错误;
D.鉴别乙醇和甲醇可以用碘仿反应,需要碘单质、NaOH,缺少试剂,不能完成,故D错误;
故选A.
点评:本题考查物质的鉴别、检验的方法及选择,为高频考点,把握物质的性质及发生的反应为解答的关键,注意反应原理及反应现象的分析,题目难度不大.

练习册系列答案
相关题目
下列表述正确的是( )
| A、1 mol氧元素 |
| B、1 mol大米 |
| C、0.5 mol H2O |
| D、0.5 mol氯 |
下列有关化学用语表示正确的是( )
A、CaH2的电子式: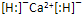 | ||
B、Cl-的结构示意图: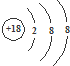 | ||
C、质子数为92、中子数为146的U原子:
| ||
D、CH2F2的电子式: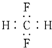 |
下列叙述正确的是( )
| A、发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B、某元素从化合态变成游离态,该元素一定被还原 |
| C、由同种分子构成的物质一定是纯净物 |
| D、电离时能生成H+的化合物一定是酸 |
下列离子或分子在溶液中能大量共存,通NO2后仍能大量共存的一组是( )
| A、K+、Na+、Br-、SiO32- |
| B、H+、Fe2+、SO42-、Cl- |
| C、K+、Ca2+、Cl-、NO3- |
| D、K+、Al3+、NH3?H2O、NO3- |
下列叙述不正确的( )
| A、金属材料分为黑色金属材料和有色金属材料 |
| B、活泼金属在空气中易与氧气反应,表面生成一层氧化膜均能保护内层金属 |
| C、硅是一种亲氧元素,在自然界中它总是与氧相互化合的 |
| D、氯是最重要的“成盐元素”,主要以NaCl的形成存在于海水和陆地的盐矿中 |
下列化学反应中,离子方程式表示正确的是( )
| A、用小苏打(NaHCO3)治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、往氢氧化钠中滴加氯化铜溶液:Cu2++2OH-=Cu(OH)2↓ |
| D、铜片插入硝酸银溶液:Cu+Ag+═Cu2++Ag |
下列说法中,正确的是( )
| A、SiO2是硅酸的酸酐,可与水化合生成硅酸 |
| B、CO2通入水玻璃中可以得到硅酸 |
| C、在高温是SiO2与Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 |
| D、SiO2是酸性氧化物,它不溶于任何酸 |
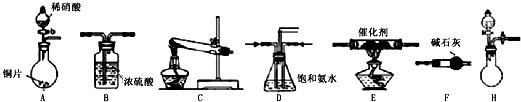
 →
→