题目内容
运用元素周期律分析下面的推断,其中不正确的是( )
| A、酸性:HClO4>HBrO4>HIO4 |
| B、砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 |
| C、在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 |
| D、稳定性:PH3>H2S>HCl |
考点:元素周期律的作用
专题:元素周期律与元素周期表专题
分析:A.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
B.卤族元素从上到下,单质的颜色逐渐加深,对应的AgX不溶于硝酸;
C.碱金属元素从上到下,单质的活泼性增强,与氧气反应可生成多种氧化物;
D.元素的非金属性越强,对应的氢化物越稳定.
B.卤族元素从上到下,单质的颜色逐渐加深,对应的AgX不溶于硝酸;
C.碱金属元素从上到下,单质的活泼性增强,与氧气反应可生成多种氧化物;
D.元素的非金属性越强,对应的氢化物越稳定.
解答:
解:A.非金属性Cl>Br>I,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故A正确;
B.卤族元素从上到下,单质的颜色逐渐加深,对应的AgX不溶于硝酸,故B正确;
C.碱金属元素从上到下,单质的活泼性增强,与氧气反应可生成多种氧化物,如过氧化物、超氧化物等,故C正确;
D.非金属性Cl>S>P,元素的非金属性越强,对应的氢化物越稳定,故D错误.
故选D.
B.卤族元素从上到下,单质的颜色逐渐加深,对应的AgX不溶于硝酸,故B正确;
C.碱金属元素从上到下,单质的活泼性增强,与氧气反应可生成多种氧化物,如过氧化物、超氧化物等,故C正确;
D.非金属性Cl>S>P,元素的非金属性越强,对应的氢化物越稳定,故D错误.
故选D.
点评:本题考查元素周期律知识,为高考常见题型,侧重于基础知识的考查,注意把握元素周期律的递变规律以及金属性、非金属性与对应单质、化合物的关系,把握比较角度,难度不大.

练习册系列答案
相关题目
下列化合物在核磁共振氢谱中能出现两组峰.且其峰面积之比为3:1的有( )
| A、乙酸异丙酯 | B、乙酸叔丁酯 |
| C、对二甲苯 | D、丙酸甲酯 |
下列表述正确的是( )
| A、1 mol氧元素 |
| B、1 mol大米 |
| C、0.5 mol H2O |
| D、0.5 mol氯 |
用括号内试剂除去下列各物质中的少量杂质,其中正确的是( )
| A、溴苯(溴):KI溶液 |
| B、苯(甲苯):酸性高锰酸钾溶液、NaOH溶液 |
| C、甲烷中乙烯(酸性高锰酸钾溶液) |
| D、苯中己烯(溴水) |
最简式相同,既不是同系物,又不是同分异构体的是( )
A、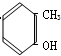 和 一CH2OH 和 一CH2OH 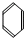 |
| B、甲酸甲酯和甲醛 |
| C、苯和乙烯 |
| D、CH3CH2OH和CH3CH2CH2OH |
下列说法正确的是( )
| A、纯碱既属于正盐又属于钠盐和碳酸盐 |
| B、根据酸的化学式中含有的氢原子个数将酸分为一元酸、二元酸、多元酸 |
| C、溶液呈电中性,胶体带有电荷 |
| D、通常情况下,铝箔在空气中燃烧易滴落下铝珠 |
下列有关化学用语表示正确的是( )
A、CaH2的电子式: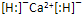 | ||
B、Cl-的结构示意图: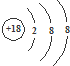 | ||
C、质子数为92、中子数为146的U原子:
| ||
D、CH2F2的电子式: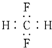 |
下列叙述正确的是( )
| A、发生化学反应时失去电子越多的金属原子,还原能力越强 |
| B、某元素从化合态变成游离态,该元素一定被还原 |
| C、由同种分子构成的物质一定是纯净物 |
| D、电离时能生成H+的化合物一定是酸 |
下列说法中,正确的是( )
| A、SiO2是硅酸的酸酐,可与水化合生成硅酸 |
| B、CO2通入水玻璃中可以得到硅酸 |
| C、在高温是SiO2与Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 |
| D、SiO2是酸性氧化物,它不溶于任何酸 |