题目内容
下列溶液中的Cl-浓度与100mL 1mol/L MgCl2溶液中的Cl-浓度相等的是( )
| A、150 mL 1mol/LNaCl溶液 |
| B、75mL 1mol/L CaCl2溶液 |
| C、150 mL 0.2mol/LKCl溶液 |
| D、75mL 1mol/LAlCl3溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:溶液中粒子的物质的量浓度=溶质的物质的物质的量浓度×离子个数,粒子的浓度与溶液的体积无关;100mL 1mol/L MgCl2溶液中的Cl-浓度为1mol/L×2=2mol/L,先计算出各选项中氯离子浓度,然后进行比较即可.
解答:
解:100mL 1mol/L MgCl2溶液中的Cl-浓度为1mol/L×2=2mol/L,
A.150 mL 1 mol?L-1NaCl溶液中氯离子浓度为:c(Cl-)=c(NaCl)=1mol/L,故A错误;
B.75 mL 1 mol?L-1CaCl2溶液中氯离子浓度为:c(Cl-)=2c(CaCl2)=1mol/L×2=2mol/L,故B正确;
C.150mL 0.2 mol?L-1KCl溶液中氯离子浓度为:c(Cl-)=c(KCl)=0.2mol/L=0.2mol/L,故C错误;
D.75mL 1mol?L-1AlCl3溶液中氯离子浓度为:c(Cl-)=3c(AlCl3)=1mol/L×3=3mol/L,故D错误;
故选B.
A.150 mL 1 mol?L-1NaCl溶液中氯离子浓度为:c(Cl-)=c(NaCl)=1mol/L,故A错误;
B.75 mL 1 mol?L-1CaCl2溶液中氯离子浓度为:c(Cl-)=2c(CaCl2)=1mol/L×2=2mol/L,故B正确;
C.150mL 0.2 mol?L-1KCl溶液中氯离子浓度为:c(Cl-)=c(KCl)=0.2mol/L=0.2mol/L,故C错误;
D.75mL 1mol?L-1AlCl3溶液中氯离子浓度为:c(Cl-)=3c(AlCl3)=1mol/L×3=3mol/L,故D错误;
故选B.
点评:本题考查物质的量浓度的计算,题目难度不大,注意明确溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少及溶质的浓度,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
关于氢键,下列说法正确的是( )
| A、DNA中的碱基互补配对是通过氢键来实现的 |
| B、氢键比分子间作用力强,所以它属于化学键 |
| C、含氢元素的化合物中一定有氢键 |
| D、H2O是一种非常稳定的化合物,这是由于氢键所致 |
下列说法正确的是( )
| A、强电解质导电能力一定强 |
| B、含强极性键的共价化合物一定是强电解质 |
| C、强电解质的饱和溶液一定是浓溶液 |
| D、强电解质的水溶液中一定存在电离平衡 |
最简式相同,既不是同系物,又不是同分异构体的是( )
A、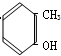 和 一CH2OH 和 一CH2OH 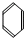 |
| B、甲酸甲酯和甲醛 |
| C、苯和乙烯 |
| D、CH3CH2OH和CH3CH2CH2OH |
下列反应中,既属于氧化还原反应,又是放热反应的是( )
| A、浓硫酸溶于水 |
| B、盐酸与氢氧化钠的反应 |
| C、灼热的碳与水蒸气的反应 |
| D、碳在少量氧气中反应生成一氧化碳 |
下列有关化学用语表示正确的是( )
A、CaH2的电子式: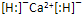 | ||
B、Cl-的结构示意图: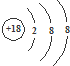 | ||
C、质子数为92、中子数为146的U原子:
| ||
D、CH2F2的电子式: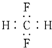 |
室温下,在PH=12的某溶液中,分别有甲、乙、丙、丁四位同学计算出由水电离出的C(OH-)的数据分别为甲:1.0×10-7mol.L-1;乙:1.0×10-6mol.L-1;丙:1.0×10-2mol.L-1;丁:1.0×10-12mol.L-1.其中你认为可能正确的数据是( )
| A、甲、乙 | B、乙、丙 |
| C、丙、丁 | D、乙、丁 |
下列离子或分子在溶液中能大量共存,通NO2后仍能大量共存的一组是( )
| A、K+、Na+、Br-、SiO32- |
| B、H+、Fe2+、SO42-、Cl- |
| C、K+、Ca2+、Cl-、NO3- |
| D、K+、Al3+、NH3?H2O、NO3- |
下列关于物质的量、摩尔质量的叙述正确的是( )
| A、0.012 kg 12C中含有约6.02×1023个碳原子 |
| B、1 mol H2O中含有2 mol氢和1 mol氧 |
| C、氢氧化钠的摩尔质量是40 g |
| D、2 mol水的摩尔质量是1 mol水的摩尔质量的2倍 |