题目内容
常温下,将熟石灰加入一定体积的水中,形成悬浊液(设pH=13),下列说法正确的是( )
| A、保持温度一定,向该浊液中加入适量的生石灰,溶液pH>13 |
| B、保持温度一定,向该浊液中加入适量的生石灰,溶液Ca2+数目减小 |
| C、向浊液中加入适量的Na2CO3或NH4Cl溶液,都会使溶液变得澄清 |
| D、将浊液加热蒸发掉一部分水,或加入pH=12的烧碱溶液,都能使浊液中固体的质量增大 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:
分析:向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,消耗水,溶液中c(Ca2+)、c(OH-)不变,由于原溶液已达到饱和,则沉淀溶解平衡向逆反应方向移动,故各离子的数目减少,但是饱和溶液的浓度只与温度有关,故浓度保持不变.
解答:
解:A.向悬浊液中加少量生石灰,发生:CaO+H2O=Ca(OH)2,反应后仍为饱和溶液,pH=13,故A错误,
B.由于原溶液已达到饱和,则沉淀溶解平衡向逆反应方向移动,故Ca2+数目减小,故B正确;
C.向浊液中加入适量的Na2CO3溶液,生成CaCO3沉淀,平衡左移,溶液仍然是浊液,故C错误;
D.将浊液加热蒸发掉一部分水,浊液中固体析出,使浊液中固体的质量减小,故D错误;
故选B.
B.由于原溶液已达到饱和,则沉淀溶解平衡向逆反应方向移动,故Ca2+数目减小,故B正确;
C.向浊液中加入适量的Na2CO3溶液,生成CaCO3沉淀,平衡左移,溶液仍然是浊液,故C错误;
D.将浊液加热蒸发掉一部分水,浊液中固体析出,使浊液中固体的质量减小,故D错误;
故选B.
点评:本题考查难溶电解质的溶解平衡,题目难度一般,要注意向悬浊液中加少量生石灰,发生的反应:CaO+H2O=Ca(OH)2,从平衡移动的角度分析.

练习册系列答案
相关题目
下列有关实验的叙述中,不合理的是( )
| A、用酸式滴定管量取25.00mL溴水 |
| B、不宜用瓷坩埚熔融氢氧化钠或碳酸钠 |
| C、测定溶液的pH时用干燥、洁净的玻璃棒蘸取溶液,滴在用蒸馏水湿润过的pH试纸上,再与标准比色卡比较 |
| D、圆底烧瓶、锥形瓶、烧杯加热时都应垫在石棉网上 |
在无色溶液中,下列离子能大量共存的是( )
| A、Na+、NH4+、NO3-、MnO4- |
| B、K +、SO42-、OH-、CO32- |
| C、K +、Fe3+、Cl-、Br- |
| D、Ba2+、Na+、OH-、CO32- |
下列表述正确的是( )
| A、NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-) |
| B、25℃时,pH=5.6的CH3COOH与CH3COONa混合溶液中,c(CH3COO-)<c(Na+) |
| C、用惰性电极电解NaOH、H2SO4、Ba(OH)2中任意一种的溶液时只生成氢气和氧气 |
| D、在水电离出的H+浓度为1×10-12 mol/L的溶液中,K+、NO3-、I-一定能大量共存 |
以下现象不涉及电化学原理的是( )
| A、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| B、纯铝制品在空气中表面逐渐失去金属光泽 |
| C、锌与稀硫酸反应时,往溶液中滴入几滴CuSO4溶液可以使反应变快 |
| D、与电源的负极相连的金属不易生锈 |
NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、1.0LPH=1的H2SO4溶液中所含H+数为0.2 NA |
B、26g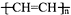 (聚乙炔)所含碳碳双键数为2 NA (聚乙炔)所含碳碳双键数为2 NA |
| C、1moAl13-团簇离子的最外层电子总数为40 NA |
| D、标准状况下,22.4LCO、CO2混合气体中所含碳原子数为2 NA |
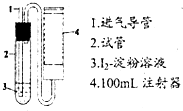 二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如图:
二氧化硫是造成大气污染的主要有害气体之一,某合作学习小组的同学拟测定某地大气中SO2的含量,实验步骤及装置如图: