题目内容
8.用NA表示阿伏加德罗常数的值,下列说法正确的是( )| A. | 标准状况下,11g CO2含有的共用电子对数为0.5NA | |
| B. | 1mol Na分别与足量的O2反应生成Na2O或Na2O2,失去的电子数均为NA | |
| C. | 通常状况下,39 g Na2O2固体中含有的离子总数为2NA | |
| D. | 滴加到沸水中的FeCl3溶液有5.6 g Fe3+发生水解,则生成的胶粒数为0.1NA |
分析 A.质量转化为物质的量,结合1个二氧化碳分子含有4对共用电子对解答;
B.Na与氧气反应无论生成氧化钠还是过氧化钠,钠都变为+1价钠离子;
C.过氧化钠阴离子为过氧根离子;
D.胶体为多个离子的集合体.
解答 解:A.标准状况下,11g CO2物质的量为$\frac{11g}{44g/mol}$=0.25mol,含有的共用电子对数为0.25mol×4×NA=NA,故A错误;
B.1molNa与足量O2反应后变为+1价,故1mol钠反应后失去NA个电子,故B正确;
C.通常状况下,39 g Na2O2固体物质的量为$\frac{39g}{78g/mol}$=0.5mol,含有的离子总数为1.5NA,故C错误;
D.胶体为多个离子的集合体,所以滴加到沸水中的FeCl3溶液有5.6 g Fe3+发生水解,则生成的胶粒数小于0.1NA,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意过氧化钠中阴离子为过氧根离子,题目难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
19.设NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A. | 4.0g 氦气中含有的最外层电子数为4NA | |
| B. | 3.9g 2H37Cl中含有的中子数为2.1NA | |
| C. | 标准状况下,11.2L丙烷中含有的非极性键数目为NA | |
| D. | 100mL 1mol•L-1 CH3COOH溶液中含有的分子数目大于0.1NA |
16.已知A、B、C、D为短周期元素构成的四种物质,它们有转化关系,且D为强电解质(其他相关物质可能省略).A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C$\stackrel{H_{2}O}{→}$D,下列说法不正确的是( )
| A. | 若A为非金属单质,则D一定为硝酸或硫酸 | |
| B. | 若A为金属单质,则A一定位于第三周期、IA族 | |
| C. | 不论A为单质还是化合物,D都有可能是同一种物质,该物质的浓溶液在常温下都能使铁和铝发生钝化 | |
| D. | 若A是共价化合物,A的水溶液一定能显碱性 |
3.下列有关实验操作、现象、解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 充分吸收了Na2SiO3饱和溶液的小木条,沥干后放在酒精灯外焰加热 | 小木条不燃烧 | Na2SiO3可能防火剂 |
| B | 将H2在充满Cl2的集气瓶中燃烧 | 集气瓶口上方有白烟生成 | H2、Cl2化合生成HCl |
| C | 将SO2通入酸性高锰酸钾溶液中 | 溶液褪色 | SO2具有漂白性 |
| D | 除去表面氧化膜的铝箔,在酒精灯上充分加热 | 铝不能滴落下来 | 铝熔点高,没能熔化 |
| A. | A | B. | B | C. | C | D. | D |
13.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | lmo1CH4中含有的电子数为9NA | |
| B. | 0.1mol•L-1的Na2S溶液中所含阴离子的数目大于0.1NA | |
| C. | 1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为2NA | |
| D. | 80℃时,1LNaCl溶液中含有OH-的数目为1×10-7NA |
20.工业上可由乙苯生产苯乙烯,反应原理如下: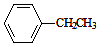 $→_{加热}^{Fe_{2}O_{3}}$
$→_{加热}^{Fe_{2}O_{3}}$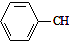 =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )
 $→_{加热}^{Fe_{2}O_{3}}$
$→_{加热}^{Fe_{2}O_{3}}$ =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )| A. | 酸性高锰酸钾溶液和溴水都可以用来鉴别乙苯和苯乙烯 | |
| B. | 乙苯、苯乙烯均能发生取代反应、加聚反应,氧化反应 | |
| C. | 乙苯的一氯取代产物有共有5种 | |
| D. | 乙苯和苯乙烯分子内共平面的碳原子数最多均为7 |
17.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 配制SnCl2溶液 | 将SnCl2固体溶于适量的蒸馏水 |
| B | AlCl3溶液制备无水AlCl3 | 向AlCl3溶液中加入盐酸后直接蒸干 |
| C | 检验溶液中的SO42-离子 | 向溶液中加入盐酸酸化的氯化钡溶液 |
| D | 除去KNO3固体中少量的NaCl | 将固体溶解后蒸发浓缩,冷却结晶,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
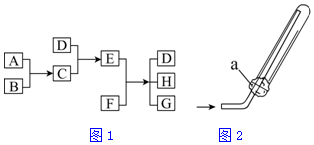 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图1所示:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转化关系如图1所示: