题目内容
15.下列各组物质相互混合反应,既有气体生成最终又有沉淀生成的组合完全正确的是( )①Ba(HCO3)2与稀H2SO4混合
②金属钠投入到FeCl3溶液中
③Na2O2投入到 Ba(NO3)2溶液混合
④Na2O2固体投入到CuSO4溶液.
| A. | ①②④ | B. | ③ | C. | ①② | D. | ①②③④ |
分析 ①碳酸氢钡和硫酸发生复分解反应;
②Na先和水反应,然后NaOH再和氯化铁发生复分解反应;
③过氧化钠先和水反应生成氢氧化钠和氧气,氢氧化钠和硝酸钡溶液不反应;
④过氧化钠先和水反应生成氢氧化钠,然后NaOH再和CuSO4反应发生复分解反应;
解答 解:①碳酸氢钡和硫酸发生复分解反应,反应方程式为:Ba(HCO3)2+H2SO4=BaSO4↓+2H2O+2CO2↑,所以符合题意,故①正确;
②Na先和水反应,然后NaOH再和氯化铁发生复分解反应,反应方程式为:6Na+6H2O+2FeCl3=2Fe(OH)3↓+6NaCl+3H2↑,所以符合题意,故②正确;
③Na2O2投入到 Ba(NO3)2溶液混合,过氧化钠先和水反应生成氢氧化钠和氧气2Na2O2+2H2O=4NaOH+O2↑,生成的氢氧化钠和硝酸钡溶液不反应无沉淀生成,故③错误;
④过氧化钠先和水反应生成氢氧化钠,然后NaOH再和CuSO4反应发生复分解反应,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑、2NaOH+CuSO4=Cu(OH)2↓+Na2SO4,所以符合题意,故④正确;
故选A.
点评 本题考查了物质间的反应,明确物质的性质是解本题关键,根据物质的性质来分析解答,熟练掌握元素化合物之间的反应,题目难度不大.

练习册系列答案
相关题目
8.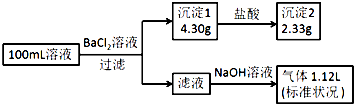 某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )
某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )
 某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )
某100mL溶液可能含有Na+、NH4+、Fe3+、CO32-、SO42-、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法不正确的是( )| A. | 原溶液一定存在CO32-和SO42-,一定不存在Fe3+ | |
| B. | 原溶液一定存在Cl-,可能存在Na+ | |
| C. | 原溶液中c(Cl-)≥0.1mol•L-1 | |
| D. | 若原溶液中不存在Na+,则c(Cl-)<0.1mol•L-1 |
3.下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A. | 1.0mol/L Na2CO3溶液:c(H2CO3)+c(HCO3-)+2 c(CO32-)=1.0mol/L | |
| B. | 1.0mol/L Na2CO3溶液:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| C. | 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-) |
10.下列反应中必须加入还原剂才能进行的是( )
| A. | H2→H2O | B. | Fe2O3→Fe2+ | C. | HCl→FeCl2 | D. | Na→NaOH |
7.下列各组离子能大量共存的是( )
| A. | H+、Na+、HCO3-、Cl- | B. | Fe3+、SCN-、Cl-、NO3- | ||
| C. | Mg2+、Cu2+、SO42-、NO3- | D. | Fe2+、SO42-、H+、NO3- |
4.化学与生产、生活密切相关.下列说法不正确的是( )
| A. | 食盐可作调味剂,也可用作食品防腐剂 | |
| B. | 二氧化硫可用于制作葡萄酒的食品添加剂 | |
| C. | 还原铁粉和生石灰均可用作食品包装袋内的脱氧剂 | |
| D. | “地沟油”禁止食用,但可用来制取肥皂 |
5.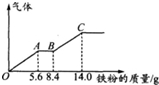 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )| A. | NO,1.5mol/L | B. | H2,1.5mol/L | C. | NO,2.5mol/L | D. | H2,2.5mol/L |



