题目内容
9.下列叙述正确的是( )| A. | N、O、F元素非金属性依次减弱 | |
| B. | Na、Mg、Al元素最高化合价依次升高 | |
| C. | Na、Li、K原子的电子层数依次增多 | |
| D. | P、Cl、S元素最高价氧化物对应的水化物酸性依次增强 |
分析 A.同一周期中,原子序数越大,非金属性越强;
B.同一周期的主族元素(O、F除外),原子序数越大,原子半径越大;
C.碱金属元素中,原子序数越大,电子层越多;
D.同一正确中,原子序数越大,非金属性越强,最高价含氧酸的酸性越强.
解答 解:A.N、O、F元素位于同一周期,原子序数逐渐增大,非金属性越强,则非金属性依次依次增强,故A错误;
B.Na、Mg、Al元素位于同一周期,原子序数逐渐增大,最外层电子数逐渐增多,其最高化合价依次升高,故B正确;
C.Li、Na、K位于同一主族,原子序数越大,电子层越多,故C错误;
D.P、S、Cl元素位于同一周期,原子序数依次增大,最高价氧化物对应的水化物酸性依次增强,故D错误;
故选B.
点评 本题考查了元素周期律的内容及应用,题目难度不大,明确原子结构与元素周期律、元素周期表的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列物质不能使酸性高锰酸钾溶液褪色的是( )
| A. | 乙烯 | B. | 乙醇 | C. | 苯 | D. | 二氧化硫 |
14.短周期元素R、W、X、Y、Z的原子序数依次增大,R原子的最外层电子数是其内层电子数的2倍,X 元素的焰色反应呈黄色,W元素和Z元素同主族,且Z元素的核电荷数是W的2倍,Y是地壳中除氧外含量最多的非金属元素.下列说法不正确的是( )
| A. | W的简单氢化物稳定性比Z的简单氢化物稳定性低 | |
| B. | Y与W形成的化合物YW2的熔点高、硬度大 | |
| C. | W与X形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| D. | Y、R、Z最高价氧化物对应水化物的酸性强弱顺序:Z>R>Y |
18.下列离子方程式正确的是( )
| A. | 向澄清石灰水中加入盐酸 Ca(OH)2+2H+→Ca2++2H2O | |
| B. | 硫化亚铁与盐酸反应 S2-+2H+→H2S↑ | |
| C. | 氯化铝溶液与过量氨水反应 Al3++3NH3•H2O→Al(OH)3↓+3NH4+ | |
| D. | 氯化亚铁溶液中通入少量氯气 Fe2++Cl2→Fe3++2Cl- |
 小明设计的探究燃烧条件的实验如图所示.请回答下列问题.
小明设计的探究燃烧条件的实验如图所示.请回答下列问题. .
.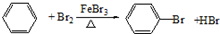 ,反应类型:取代反应.
,反应类型:取代反应.