题目内容
17.按下列要求书写反应方程式,有要求的要注明反应类型.(1)乙烯与Br2的反应:CH2=CH2+Br2→CH2Br-CH2Br,反应类型:加成反应.
(2)乙烯制聚乙烯:
 .
.(3)苯与液溴的反应:
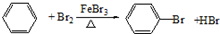 ,反应类型:取代反应.
,反应类型:取代反应.(4)乙醇与金属钠的反应:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑.
(5)乙醇的催化氧化反应:2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O.
分析 (1)乙烯的与Br2的加成反应生成1,2-二溴乙烷;
(2)乙烯中含双键,可发生加聚反应生成聚乙烯;
(3)苯与液溴在溴化铁做催化剂条件下发生取代反应生成溴苯和溴化氢;
(4)乙醇与与金属钠反应生成乙醇钠和氢气,断开羟基上的氢氧键;
(5)乙醇催化氧化生成乙醛和水.
解答 解:(1)乙烯含有碳碳双键,与Br2发生加成反应,生成1,2-二溴乙烷,方程式为:CH2=CH2+Br2→CH2Br-CH2Br,
故答案为:CH2=CH2+Br2→CH2Br-CH2Br;加成反应;
(2)乙烯在催化剂条件下生成聚乙烯,化学方程式为 ,
,
故答案为: ;
;
(3)在催化剂的作用下,苯环上的氢原子被溴原子所取代,生成溴苯,同时有溴化氢生成,反应为: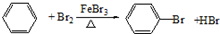 ,
,
故答案为: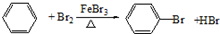 ;取代反应;
;取代反应;
(4)乙醇与与金属钠反应生成乙醇钠和氢气,断开羟基上的氢氧键,反应方程式为2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
(5)乙醇与氧气发生催化氧化,CH3CH2OH得到了氧同时失去氢,生成乙醛和水:2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu或Ag}$2CH3CHO+2H2O.
点评 本题考查了有机化学方程式书写,为高频考点,把握物质的性质及发生的化学反应为解答的关键,题目难度不大.

练习册系列答案
相关题目
18.天津市场销售的某种食用精制盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处):
1KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O
(2)上述反应生成的I2可用四氯化碳检验,向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+.
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体.
以上设计中遗漏的操作及在上述步骤中的位置是在步骤b后,增加操作:将分液漏斗充分振荡后静置.
(3)已知:I2+2S2O32-═2I-+S4O62-.
某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是滴最后一滴溶液,由蓝色恰好变为无色,且半分钟内不变色.
②b中反应所产生的I2的物质的量是1.0×10-5mol.
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)$\frac{423}{w}$mg/kg.
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
1KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O
(2)上述反应生成的I2可用四氯化碳检验,向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+.
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体.
以上设计中遗漏的操作及在上述步骤中的位置是在步骤b后,增加操作:将分液漏斗充分振荡后静置.
(3)已知:I2+2S2O32-═2I-+S4O62-.
某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是滴最后一滴溶液,由蓝色恰好变为无色,且半分钟内不变色.
②b中反应所产生的I2的物质的量是1.0×10-5mol.
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)$\frac{423}{w}$mg/kg.
8.如图曲线的变化趋势完全正确的一组是( )
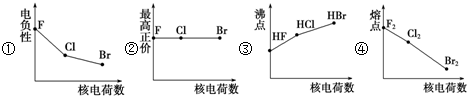

| A. | ①②③④ | B. | ②③④ | C. | ① | D. | ①②③ |
5.下列解释事实的离子方程式不正确的是( )
| A. | 粗铜精炼时,阴极质量增加:Cu2++2e-═Cu | |
| B. | 明矾可用作净水剂:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | 用食醋除去水壶中的水垢(CaCO3):2CH3COOH+CaCO3═Ca2++2CH3COO-+CO2↑+H2O | |
| D. | 向氢氧化镁浊液中滴入酚酞溶液,溶液变红:Mg(OH)2(s)?Mg2+(aq)+2OH- (aq) |
12.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图.下列说法不正确的是( )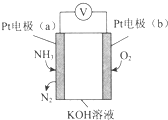

| A. | 溶液中OH-向电极a移动 | |
| B. | O2在电极b上发生还原反应 | |
| C. | 反应消耗的NH3与O2的物质的量之比为4:5 | |
| D. | 电极a的反应式为2NH3-6e-+6OH-═N2+6H2O |
2.下列说法正确的是( )
| A. | 可逆反应达到化学平衡状态时,正、逆反应的速率都为0 | |
| B. | 催化剂可以使不起反应的物质发生反应 | |
| C. | 可以找到一种催化剂使水变成油 | |
| D. | 增大反应物的浓度、提高反应温度都能增大反应速率 |
9.下列叙述正确的是( )
| A. | N、O、F元素非金属性依次减弱 | |
| B. | Na、Mg、Al元素最高化合价依次升高 | |
| C. | Na、Li、K原子的电子层数依次增多 | |
| D. | P、Cl、S元素最高价氧化物对应的水化物酸性依次增强 |
6.下列离子在溶液中能常量共存的是( )
| A. | K+ H+ Fe2+ NO3- | B. | H+ Al3+ SO42- Cl- | ||
| C. | Na+ Al3+ HCO3- Cl- | D. | Na+ NH4+ OH- CO32- |
7.将两块相同的纯铁片,一片放入冷的浓H2SO4 中浸泡一段时间后,取出洗净,另一片未作任何处理,而后两块铁片分别放入硫酸铜溶液中,则下列说法正确的是( )
| A. | 两块铁片上均有铜析出 | B. | 两块铁片上均无铜析出 | ||
| C. | 浸过浓H2SO4 的铁片上有铜析出 | D. | 浸过浓H2SO4 的铁片上无铜析出 |