题目内容
14. 小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验.
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验.实验过程:
Ⅰ、按图组装仪器,检查装置的气密性;
Ⅱ、将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3g;
Ⅲ、关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
Ⅳ、称得装置B的质量为m4g、装置C的质量为m5g.
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O、Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O.
(2)装置C的作用为吸收反应生成的水蒸气.装置D的作用为吸收反应生成的二氧化碳.
(3)实验过程中通入N2的目的是使装置中的二氧化碳和水蒸气全部排出被装置BC全部吸收.
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是bce(填选项字母).
| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m2、m5 |
分析 (1)小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),装置A中发生反应为碳酸氢钠受热分解生成碳酸钠、二氧化碳和水;碳酸钠晶体失水生成碳酸钠和水;
(2)装置B中的浓硫酸具有吸水性,可以吸收气体中的水蒸气;装置C中是碱石灰用来吸收碳酸氢钠分解生成的二氧化碳气体;
(3)实验过程中通入N2的目为把生成的水蒸气和二氧化碳气体全部赶到BC装置中完全吸收;
(4)由题意可知生成水的质量是(m4-m2)g,生成二氧化碳的质量为(m5-m3)g,原样品质量为m1g,可以利用生成的二氧化碳质量计算碳酸氢钠的质量,也可以由生成水的质量列方程组计算碳酸氢钠的质量,若再知道原样品质量即可计算碳酸氢钠的质量分数,所以利用ce组数据能计算,利用B组数据可以由生成二氧化碳的质量计算碳酸氢钠质量,再由生成水的质量计算得到碳酸钠晶体质量,进一步可以求碳酸氢钠质量分数;
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,可以利用二氧化碳质量计算,利用实验中所提供的数据得到准确的w(NaHCO3).
解答 解:(1)小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),装置A中发生反应为碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,反应的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O;碳酸钠晶体失水生成碳酸钠和水,反应的化学方程式为:Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O;
故答案为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O;
(2)装置B中的浓硫酸具有吸水性,可以吸收气体中的水蒸气;装置C中是碱石灰用来吸收碳酸氢钠分解生成的二氧化碳气体;
故答案为:吸收反应生成的水蒸气;吸收反应生成的二氧化碳;
(3)实验过程中通入N2的目为把生成的水蒸气和二氧化碳气体全部赶到BC装置中完全吸收;
故答案为:使装置中的二氧化碳和水蒸气全部排出被装置BC全部吸收;
(4)由题意可知生成水的质量是(m4-m2)g,生成二氧化碳的质量为(m5-m3)g,原样品质量为m1g,可以利用生成的二氧化碳质量计算碳酸氢钠的质量,也可以由生成水的质量列方程组计算碳酸氢钠的质量,若再知道原样品质量即可计算碳酸氢钠的质量分数,所以利用ce组数据能计算,利用B组数据可以由生成二氧化碳的质量计算碳酸氢钠质量,再由生成水的质量计算得到碳酸钠晶体质量,进一步可以求碳酸氢钠质量分数;
故答案为:bce;
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,可以利用二氧化碳质量计算,利用实验中所提供的数据得到准确的w(NaHCO3)=$\frac{\frac{{m}_{5}-m{\;}_{3}}{44}×84}{{m}_{1}}$×100%=$\frac{42({m}_{5}-{m}_{3})}{11m{\;}_{1}}$×100%;
故答案为:$\frac{42({m}_{5}-{m}_{3})}{11m{\;}_{1}}$×100%.
点评 本题考查了物质组成的实验探究方法和实验过程分析判断,主要是实验流程的理解应用,掌握基础是关键,题目难度中等.

| A. | 向100mL 1mol/L盐酸溶液中加入4g NaOH固体 | |
| B. | 向100mL 1mol/L的醋酸溶液中通适量NH3气体 | |
| C. | 向饱和和澄清石灰水中通少量CO2气体 | |
| D. | 通足量的氯气于氢氧化钠溶液中 |
| A. | 用高锰酸钾溶液滴定Na2SO3溶液至终点,滴入最后一滴高锰酸钾溶液,溶液颜色恰好由紫红色变为无色且半分钟不变色 | |
| B. | 燃料电池制作的实验中,石墨棒用海绵包裹是为了更好的固定电极 | |
| C. | pH试纸在检测溶液时不能湿润,使用石蕊试纸检测气体时需要湿润并粘在洁净玻璃棒的一端 | |
| D. | 海带中提取碘,可将灰化后的海带加水煮沸一段时间后过滤,在滤液中加入稀硫酸后转移到分液漏斗中用CCl4萃取分离 |
| A. | 氟化氢的电子式: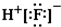 | B. | HClO的结构式:H-Cl-O | ||
| C. | 甲基的电子式 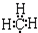 | D. | 基态氧原子L层电子排布图: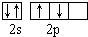 |
| A. | SiO2 是酸性氧化物,不溶于水,也不能与任何酸发生反应 | |
| B. | Na2O、Na2O2组成元素虽然相同,但与H2O、CO2等反应的产物不完全相同 | |
| C. | CO、SO2、NO、NO2都是对大气产生污染的气体,他们在空气中都能稳定存在 | |
| D. | 浓硫酸可用于干燥氢气、氯化氢、碘化氢等气体,但不能干燥氨气、二氧化氮气体 |
| A. | 436kJ | B. | 557kJ | C. | 872kJ | D. | 181kJ |
Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
(1)基态Ti3+的未成对电子数有1个.
(2)LiBH4由Li+和BH4-构成,LiBH4中不存在的作用力有C(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
(3)Li、B、H元素的电负性由大到小排列顺序为H>B>Li.
(4)分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是BC(填标号).
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)钾、镁、氟形成的某化合物的晶体结构为K+在立方晶胞的中心,Mg2+在晶胞的8个顶角,F-处于晶胞的棱边中心.由钾、镁、氟形成的该化合物的化学式为KMgF3,每个K+与12个F-配位.
(6)判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示:含氧酸酸性强弱与非羟基氧原子数的关系
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 | Cl-OH |  |  |  |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 .H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
.H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:①H3PO3+2NaOH=Na2HPO3+2H2O,
②H3AsO3+3NaOH=Na3AsO3+3H2O.
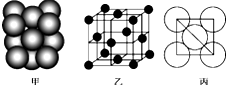 铜单质晶体中原子的堆积方式如图甲所示,其晶胞如图乙所示,原子之间相互位置关系的平面图如图丙所示.
铜单质晶体中原子的堆积方式如图甲所示,其晶胞如图乙所示,原子之间相互位置关系的平面图如图丙所示.