题目内容
5.有关下列说法正确的是( )| A. | 用高锰酸钾溶液滴定Na2SO3溶液至终点,滴入最后一滴高锰酸钾溶液,溶液颜色恰好由紫红色变为无色且半分钟不变色 | |
| B. | 燃料电池制作的实验中,石墨棒用海绵包裹是为了更好的固定电极 | |
| C. | pH试纸在检测溶液时不能湿润,使用石蕊试纸检测气体时需要湿润并粘在洁净玻璃棒的一端 | |
| D. | 海带中提取碘,可将灰化后的海带加水煮沸一段时间后过滤,在滤液中加入稀硫酸后转移到分液漏斗中用CCl4萃取分离 |
分析 A.高锰酸钾溶液呈紫色,Na2SO3溶液与高锰酸钾溶液恰好反应时,溶液是无色的,当高锰酸钾过量时溶液呈紫色;
B.增大反应物接触面积,加快反应速率;
C.pH试纸测定溶液pH时不能湿润,否则易导致溶液浓度降低,pH测定值有影响;使用石蕊试纸检测气体时需要湿润并粘在洁净玻璃棒的一端,根据试纸颜色判断气体成分;
D.需要将碘离子氧化为碘单质,然后用四氯化碳萃取碘.
解答 解:A、当Na2SO3被消耗完毕时,再滴加高锰酸钾溶液则出现紫色,所以终点时溶液由无色变为紫色,故A错误;
B.增大反应物接触面积,加快反应速率,墨棒用海绵包裹是为了增大反应物接触面积,加快反应速率,故B错误;
C.pH试纸测定溶液pH时不能湿润,否则易导致溶液浓度降低,导致pH测定值不准确;使用石蕊试纸检测气体时需要湿润并粘在洁净玻璃棒的一端,根据试纸颜色判断气体成分,故C正确;
D.需要将碘离子氧化为碘单质,然后用四氯化碳萃取碘,需要用双氧水将碘离子氧化为碘,然后用四氯化碳萃取碘,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及氧化还原反应滴定、反应速率影响因素、pH试纸使用方法、海带中碘的提取等知识点,明确实验原理及实验操作规范性是解本题关键,易错选项是D,题目难度中等.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
3.可逆反应N2O4?2NO2△H>0在密闭容器中反应,达到平衡状态,要使混合气体颜色加深,可采取的方法是( )
①选用合适的催化剂; ②缩小体积; ③升高温度; ④增大N2O4的浓度.
①选用合适的催化剂; ②缩小体积; ③升高温度; ④增大N2O4的浓度.
| A. | ③④ | B. | ①②③ | C. | ②③④ | D. | ①④ |
4.据报道,科学家通过对稻壳进行控制性焚烧热解,从中提取一种叫做生物质纳米结构二氧化硅的超高活性材料,将少量这种材料掺入混凝土中,即可制备出超高强度的高性能混凝土.下列关于二氧化硅的说法中,正确的是( )
| A. | 二氧化硅溶于水显酸性,所以二氧化硅属于酸性氧化物 | |
| B. | 将二氧化碳通入硅酸钠溶液可以得到硅酸 | |
| C. | 因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强 | |
| D. | 二氧化硅是酸性氧化物,它不溶于任何酸 |
8.用NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 1molNaC1中阴、阳离子数之和为2NA | B. | 0.3mol NH3中所含质子数为3NA | ||
| C. | 0.2molNa2SO4所带电荷数为0.2NA | D. | 2mol HNO3中所含原子数为10NA |
10.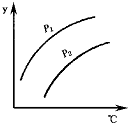 如图表示不同温度和压强下,对可逆反应2L(气)?2M(气)+N(气)△H>0平衡状态的影响(p1<p2),图中y轴表示的意义是( )
如图表示不同温度和压强下,对可逆反应2L(气)?2M(气)+N(气)△H>0平衡状态的影响(p1<p2),图中y轴表示的意义是( )
 如图表示不同温度和压强下,对可逆反应2L(气)?2M(气)+N(气)△H>0平衡状态的影响(p1<p2),图中y轴表示的意义是( )
如图表示不同温度和压强下,对可逆反应2L(气)?2M(气)+N(气)△H>0平衡状态的影响(p1<p2),图中y轴表示的意义是( )| A. | 一定条件下L的转化率 | B. | 气体混合物的平均摩尔质量 | ||
| C. | 气体混合物中L的体积分数 | D. | 气体L的物质的量 |
17.下列说法不正确的是( )
| A. | 分子组成相差一个或若干个CH2原子团的化合物必定互为同系物 | |
| B. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| C. | 具有相同通式的有机物不一定互为同系物 | |
| D. | 两个相邻同系物的相对分子质量数值一定相差14 |
14.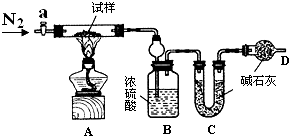 小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验.
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验.
实验过程:
Ⅰ、按图组装仪器,检查装置的气密性;
Ⅱ、将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3g;
Ⅲ、关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
Ⅳ、称得装置B的质量为m4g、装置C的质量为m5g.
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O、Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O.
(2)装置C的作用为吸收反应生成的水蒸气.装置D的作用为吸收反应生成的二氧化碳.
(3)实验过程中通入N2的目的是使装置中的二氧化碳和水蒸气全部排出被装置BC全部吸收.
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是bce(填选项字母).
(5)实验结束后发现装置A中硬质玻璃管右端有水珠,你认为利用实验中所提供的数据还能否得到准确的w(NaHCO3),若能,则w(NaHCO3)的计算式为:$\frac{42({m}_{5}-{m}_{3})}{11m{\;}_{1}}$×100%.
 小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验.
小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3•10H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验.实验过程:
Ⅰ、按图组装仪器,检查装置的气密性;
Ⅱ、将试样m1g放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3g;
Ⅲ、关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
Ⅳ、称得装置B的质量为m4g、装置C的质量为m5g.
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O、Na2CO3•10H2O$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+10H2O.
(2)装置C的作用为吸收反应生成的水蒸气.装置D的作用为吸收反应生成的二氧化碳.
(3)实验过程中通入N2的目的是使装置中的二氧化碳和水蒸气全部排出被装置BC全部吸收.
(4)用下列各项所提供的数据能计算出w(NaHCO3)的是bce(填选项字母).
| 序号 | a | b | c | d | e |
| 数据 | m1、m2、m3 | m2、m3、m4、m5 | m1、m2、m4 | m1、m4、m5 | m1、m2、m5 |
15.已知Ksp(CaSO4)=9.0×10-6,Ksp(CaCO3)=5.0×10-9,Ksp(CaF2)=1.5×10-10.某溶液中含有SO42-、CO32-和F-,浓度均为0.010mol/L,向该溶液中逐滴加入0.010mol/L的CaCl2溶液时,三种阴离子产生沉淀的先后顺序为( )
| A. | SO42-、CO32-、F- | B. | CO32-、SO42-、F- | C. | CO32-、F-、SO42- | D. | F-、CO32-、SO42- |