题目内容
下列反应不能够发生的是( )
| A、2Fe+3I2=2FeI3 |
| B、3Br2+6FeCl2=2FeBr3+4FeCl3 |
| C、Cl2+2KBr=2KCl+Br2 |
| D、2FeCl3+2KI=2FeCl2+2KCl+I2 |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:根据化学方程式,只要根据氧化还原反应中还原剂的还原性强于还原产物的还原性,氧化剂的氧化性强于氧化产物的氧化性得出的结果符合题干已知条件的,说明反应成立.
解答:
解:A、根据2Fe+3I2=2FeI3可知氧化性是I2>Fe3+,不符合题干已知条件,所以化学方程式不成立,故A选;
B、根据3Br2+6FeCl2=2FeBr3+4FeCl3可知氧化性是Br2>Fe3+,符合题干已知条件,所以化学方程式成立,故B不选;
C、根据Cl2+2KBr=2KCl+Br2可知氧化性是Cl2>Br2,符合题干已知条件,所以化学方程式成立,故C不选;
D、根据2FeCl3+2KI=2FeCl2+2KCl+I2可知氧化性是Fe3+>I2,符合题干已知条件,所以化学方程式成立,故D不选;
故选A.
B、根据3Br2+6FeCl2=2FeBr3+4FeCl3可知氧化性是Br2>Fe3+,符合题干已知条件,所以化学方程式成立,故B不选;
C、根据Cl2+2KBr=2KCl+Br2可知氧化性是Cl2>Br2,符合题干已知条件,所以化学方程式成立,故C不选;
D、根据2FeCl3+2KI=2FeCl2+2KCl+I2可知氧化性是Fe3+>I2,符合题干已知条件,所以化学方程式成立,故D不选;
故选A.
点评:本题考查氧化性强弱的判断规律:氧化剂的氧化性强于氧化产物的氧化性,侧重于基础知识的考查,难度不大.

练习册系列答案
相关题目
某有机物的结构简式如图,该物质1mol与足量的NaOH溶液反应,消耗NaOH的物质的量为( )
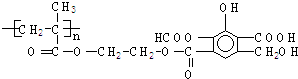
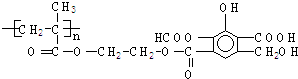
| A、5 mol |
| B、6 mol |
| C、5n mol |
| D、6n mol. |
下列说法正确的是( )
| A、1mol CO和1mol N2所含分子数相等,质量相等,它们所占的体积也相等 |
| B、22.4L H2和71g Cl2恰好反应生成2mol HCl |
| C、非标准状况下,1mol气体的体积有可能是22.4L |
| D、1mol HCl和1mol H2O在标准状况下的体积都约是22.4L |
 石墨烯(graphene)是目前科技研究的热点,可看作将石墨的层状结构一层一层的剥开得到的单层碳原子.将氢气加入到石墨烯排列的六角晶格中可得最薄的导电材料石墨烷(graphane,如图),下列说法中正确的是(NA表示阿伏伽德罗常数)( )
石墨烯(graphene)是目前科技研究的热点,可看作将石墨的层状结构一层一层的剥开得到的单层碳原子.将氢气加入到石墨烯排列的六角晶格中可得最薄的导电材料石墨烷(graphane,如图),下列说法中正确的是(NA表示阿伏伽德罗常数)( )| A、石墨烯与石墨烷互为同素异形体 |
| B、石墨烯转变为石墨烷可看作取代反应 |
| C、12g石墨烯所含碳碳键数目为1.5NA |
| D、12g石墨烯完全转变为石墨烷需氢气11.2L |
实验室需用2mol/L氯化钠溶液450mL,配置时应选用容量瓶的规格和称取氯化钠的质量分别是( )
| A、450mL,52.7g |
| B、500mL,58.5g |
| C、1000mL,117g |
| D、任意规格,111.2g |
下列表示物质结构的化学用语或模型图正确的是( )
| A、乙醇的分子式:CH3CH2OH | ||
B、二氧化碳的电子式: | ||
C、乙烷的球棍模型 | ||
D、中子数为20的氯原子:
|
下列说法一定正确的是( )
| A、周期表中同主族元素单质的熔点从上到下逐渐增高 |
| B、16g石墨与8g CH4所含共价键数目相等 |
| C、钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 |
| D、若将AlCl3溶液、Na2SO3溶液蒸干并灼烧可分别得到AlCl3和Na2SO3 |
几种短周期元素的原子半径及主要化合价如下表:
下列叙述不正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| A、X、Y元素的金属性:X比Y强 |
| B、一定条件下,Z单质与W的常见单质直接生成ZW |
| C、Y的最高价氧化物对应的水化物能溶于的Z最高价氧化物对应的水化物的稀溶液中 |
| D、一定条件下,W单质可以和Z氢化物反应直接生成ZW2 |