题目内容
下列表示物质结构的化学用语或模型图正确的是( )
| A、乙醇的分子式:CH3CH2OH | ||
B、二氧化碳的电子式: | ||
C、乙烷的球棍模型 | ||
D、中子数为20的氯原子:
|
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.乙醇的分子式只需要表示出含有的元素种类及数目,不需要写出官能团;
B.二氧化碳为共价化合物,分子中存在两个碳氧双键;
C.根据比例模型与球棍模型的表示方法进行判断;
D.氯原子的核电荷数为17,中子数为20的氯原子的质量数为37.
B.二氧化碳为共价化合物,分子中存在两个碳氧双键;
C.根据比例模型与球棍模型的表示方法进行判断;
D.氯原子的核电荷数为17,中子数为20的氯原子的质量数为37.
解答:
解:A.乙醇分子中存在2个C、6个H和1个O,乙醇的分子式为:C2H6O,故A错误;
B.二氧化碳为共价化合物,分子中存在两个碳氧双键,氧原子和碳原子的最外层都达到8电子稳定结构,二氧化碳正确的电子式为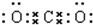 ,故B错误;
,故B错误;
C.乙烷分子中存在1个碳碳键、6个碳氢键,碳原子的原子半径大于氢原子,用短棍表示共价键,用小球表示乙烷中的各原子,则乙烷的球棍模型为 ,故C正确;
,故C正确;
D.氯元素的核电荷数为17,中子数为20的氯原子的质量数为37,该氯原子正确的表示方法为:1737Cl,故D错误;
故选C.
B.二氧化碳为共价化合物,分子中存在两个碳氧双键,氧原子和碳原子的最外层都达到8电子稳定结构,二氧化碳正确的电子式为
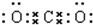 ,故B错误;
,故B错误;C.乙烷分子中存在1个碳碳键、6个碳氢键,碳原子的原子半径大于氢原子,用短棍表示共价键,用小球表示乙烷中的各原子,则乙烷的球棍模型为
 ,故C正确;
,故C正确;D.氯元素的核电荷数为17,中子数为20的氯原子的质量数为37,该氯原子正确的表示方法为:1737Cl,故D错误;
故选C.
点评:本题考查了分子式、电子式、球棍模型、元素符号等化学用语的表示方法判断,题目难度中等,注意掌握常见化学用语的概念及正确表示方法,明确电子式、分子式、结构式、结构简式等化学用语之间的区别.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
下列电离方程式书写正确的是( )
| A、NaHCO3=Na++H++CO32- |
| B、HF?H++F- |
| C、H2CO3?2H++CO32- |
| D、CH3COONH4?CH3COO-+NH4+ |
共价键、离子键和分子间作用力是构成物质的微粒间的不同作用方式.下列物质通过分子间作用力形成的是( )
| A、石墨 | B、氯化钠 |
| C、氢氧化钠 | D、干冰 |
下列反应不能够发生的是( )
| A、2Fe+3I2=2FeI3 |
| B、3Br2+6FeCl2=2FeBr3+4FeCl3 |
| C、Cl2+2KBr=2KCl+Br2 |
| D、2FeCl3+2KI=2FeCl2+2KCl+I2 |
下列物质中,属于酸性氧化物但不溶于水的是( )
| A、三氧化硫 | B、二氧化硅 |
| C、二氧化碳 | D、氧化铁 |
下列各组物质中互称为同分异构体的是( )
| A、乙醇(CH3CH2OH)与二甲醚(CH3OCH3) |
| B、水与重水 |
| C、红磷与白磷 |
| D、O2与O3 |
下列说法正确的是( )
| A、含有离子键的化合物一定是离子化合物 |
| B、含有共价键的化合物一定是共价化合物 |
| C、全部由非金属元素组成的化合物一定是共价化合物 |
| D、H2SO4溶于水能电离出H+和SO42-,所以H2SO4是离子化合物 |
下列表示物质结构的化学用语或模型正确的是( )
A、苯分子的比例模型: |
B、CO2的电子式: |
C、Cl-离子的结构示意图: |
| D、乙烯的结构式:CH2=CH2 |
下列关于电解质叙述正确的是( )
| A、CO2溶于水能部分电离,故CO2属于弱电解质 |
| B、溶于水后能电离出氢离子的化合物都是酸 |
| C、硫酸钡难溶于水,但硫酸钡属强电解质 |
| D、强电解质溶液的导电性比弱电解质溶液的导电性强 |