题目内容
实验室需用2mol/L氯化钠溶液450mL,配置时应选用容量瓶的规格和称取氯化钠的质量分别是( )
| A、450mL,52.7g |
| B、500mL,58.5g |
| C、1000mL,117g |
| D、任意规格,111.2g |
考点:溶液的配制
专题:物质的量浓度和溶解度专题
分析:配制450mL溶液,由于实验室中没有450mL的容量瓶,只能选用规格为500mL的容量瓶进行配制,实际上配制的是500mL 2mol/L的氢氧化钠溶液,根据mnM=cVM计算出需要氢氧化钠的质量即可.
解答:
解:实验室需用2mol/L氯化钠溶液450mL,只能选用500mL容量瓶配制,实际上配制的是500mL 2mol/L的氯化钠溶液,
配制该溶液需要氯化钠的质量为:m(NaCl)=cVM=58.5g/mol×2mol/L×0.5L=58.5g,
所以配置时应选用容量瓶的规格和称取氯化钠的质量分别是:500mL、58.5g,
故选B.
配制该溶液需要氯化钠的质量为:m(NaCl)=cVM=58.5g/mol×2mol/L×0.5L=58.5g,
所以配置时应选用容量瓶的规格和称取氯化钠的质量分别是:500mL、58.5g,
故选B.
点评:本题考查了配制一定物质的量浓度的溶液,题目难度不大,注意掌握配制一定物质的量浓度的溶液方法,要求学生能够根据配制过程正确选用所需仪器及其规格.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
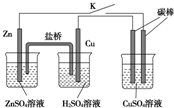 用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1mol CuO后CuSO4溶液恰好恢复到反应前的浓度和pH.下列说法中不正确的是( )
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1mol CuO后CuSO4溶液恰好恢复到反应前的浓度和pH.下列说法中不正确的是( )| A、铜棒为正极,其电极反应式为:2H++2e-═H2↑ |
| B、烧杯右侧碳棒为阴极,其电极表面有红色物质析出 |
| C、反应中消耗锌的质量为13g |
| D、导线中通过电子的物质的量为0.2 mol |
太阳能电池板面对太阳时,一部分电能直接供给“天宫一号”,一部分电能则储存在电池里,供背离太阳时使用.“天宫一号”使用的是镍氢电池,电解质溶液显碱性.其反应方程式为:LaNi5+Ni(OH)2
LaNi5H+NiOOH.下列有关说法不正确的是( )
| 放电 |
| 充电 |
| A、放电时镍被还原 |
| B、放电时负极LaNi5H+OH--e-═LaNi5+H2O |
| C、充电时OH-向阴极移动 |
| D、充电时每消耗1mol Ni(OH)2转移1mol电子 |
中学化学教材中有大量的数据材料.下面是某学生对数据的利用情况,其中正确的是( )
| A、利用熔变数据就可以判断反应的自发性 |
| B、利用pH与7的大小关系来判断溶液的酸碱性 |
| C、利用第一电离能数据,可判断同周期元素的金属性强弱 |
| D、利用健能、键角和键长等数据可以推测化合物的热稳定性 |
下列反应不能够发生的是( )
| A、2Fe+3I2=2FeI3 |
| B、3Br2+6FeCl2=2FeBr3+4FeCl3 |
| C、Cl2+2KBr=2KCl+Br2 |
| D、2FeCl3+2KI=2FeCl2+2KCl+I2 |
下列各组元素中,原子半径依次增大的是( )
| A、C、N、B |
| B、O、S、Na |
| C、I、Br、Cl |
| D、Al、Si、P |
下列各组物质中互称为同分异构体的是( )
| A、乙醇(CH3CH2OH)与二甲醚(CH3OCH3) |
| B、水与重水 |
| C、红磷与白磷 |
| D、O2与O3 |
S2Cl2是橙黄色液体.少量泄漏会产生窒息性气味,喷水雾可减慢挥发,并产生酸性悬浊液.该分子的结构中两个Cl位于以两个S连线为交线的两个平面内,下列关于S2Cl2的说法正确的是( )
| A、为非极性分子 |
| B、该分子中S采取sp杂化 |
| C、分子中既含σ键又含π键 |
| D、与水反应的化学方程式可能为2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
红磷在一定条件下能转变成白磷,同时释放出一定的热能,据此下列结论正确的是( )
| A、红磷和白磷互称同位素 |
| B、相同量的白磷比红磷的总能量低 |
| C、该反应是吸热反应 |
| D、红磷比白磷稳定 |