题目内容
V L硫酸铝溶液含有n mol Al3+,则溶液中SO42-物质的量的浓度为 .
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:硫酸铝溶液中存在c(SO42-)=
c(Al3+),结合c=
计算.
| 3 |
| 2 |
| n |
| V |
解答:
解:n(Al3+)=
=
mool/L,c(SO42-)=
c(Al3+)=
mol/L,
故答案为:
mol/L.
| nmol |
| V |
| n |
| V |
| 3 |
| 2 |
| 3n |
| 2V |
故答案为:
| 3n |
| 2V |
点评:本题考查物质大量的浓度的简单计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意相关计算公式的运用以及离子浓度的关系,难度不大.

练习册系列答案
相关题目
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化如图所示.下列说法中正确是( )


| A、30 min~40 min间该反应使用了催化剂 |
| B、反应方程式中的x=1,正反应为吸热反应 |
| C、30~40min改变的条件是将容器的体积扩大至原来的2倍 |
| D、在25min、35min、55min时化学平衡常数分别为K1、K2、K3,则K1=K2>K3 |
用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、0.1mol/L稀硫酸100mL中含有SO42- 个数为0.1NA |
| B、1.7g NH3所含的电子数目为10NA |
| C、2g H2所含原子数目为2NA |
| D、标准状况下,33.6LSO3含有SO3分子数为1.5NA |
某学习小组设计如下实验方案,相关推测不合理的是( )


| A、试管②滴入酚酞后溶液可能变浅红 |
| B、试管③滴入FeCl3溶液后有红褐色沉淀生成 |
| C、试管③中的变化是物理变化 |
| D、上述反应说明Fe(OH)3溶解性小于Mg(OH)2 |
下列说法正确的是( )
A、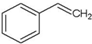 能使溴水褪色,但不能是酸性高锰酸钾溶液褪色 能使溴水褪色,但不能是酸性高锰酸钾溶液褪色 |
| B、乙烯能和溴水、酸性高锰酸钾溶液发生加成反应使之褪色 |
| C、气态烃CxHy与适量O2恰好完全反应,如果反应前后气体体积不变(温度>100℃),则 y=4 |
| D、相同质量的烃,完全燃烧,消耗O2越多,烃中含碳的质量分数越高 |
下列说法正确的是( )
| A、纯碱不是碱 |
| B、食盐不是盐 |
| C、火碱不是碱 |
| D、干冰不是冰 |
下列关于物质的用途,不正确的是( )
| A、小苏打可用于治疗胃酸过多 |
| B、Cl2可与石灰乳反应制取漂白粉 |
| C、镁铝合金可用作制造飞机的材料 |
| D、铁制容器不能用于贮存浓硫酸 |
 实验室用NaOH和FeSO4制取Fe(OH)2时,Fe(OH)2很容易被氧化,若采用如图所示装置制取,可以得到较纯净的Fe(OH)2.
实验室用NaOH和FeSO4制取Fe(OH)2时,Fe(OH)2很容易被氧化,若采用如图所示装置制取,可以得到较纯净的Fe(OH)2.