题目内容
13.化学与材料、生活和环境密切相关.下列有关说法不正确的是( )| A. | 煤炭经气化、液化和干馏等过程,可获得清洁能源和重要的化工原料 | |
| B. | 机动车实行限行措施是减少雾霾的途径之一 | |
| C. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 | |
| D. | 神舟10号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是单晶硅 |
分析 A.煤通过气化、液化和干馏等可获得水煤气、甲醇以及苯等有机物;
B.机动车实行限行,可减少汽油、柴油的使用,从而减少固体颗粒物排放;
C.常温下铝能与氧气反应生成致密的氧化膜,可保护内部Al;
D.Si为常见的半导体材料,太阳能电池的材料是硅单质.
解答 解:A.煤的气化是煤在氧气不足的条件下进行部分氧化形成H2、CO等气体的过程;煤的液化是将煤与H2在催化剂作用下转化为液体燃料或者利用煤产生的H2和CO通过化学合成产生液体燃料或者其他液体化工产品的过程;煤的干馏是指隔绝空气加强热,使煤分解的过程,可以得到很多重要的化工原料,故A正确;
B.机动车实行限行,可减少汽油、柴油的使用,从而减少固体颗粒物排放,则机动车实行限行措施是减少雾霾的途径之一,故B正确;
C.常温下铝能与氧气反应生成致密的氧化膜,可保护内部Al,则日常生活中人们大量使用铝制品,故C错误;
D.Si为常见的半导体材料,太阳能电池的材料是硅单质,Si电池板可将光能转换为电能,故D正确;
故选C.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、化石能源应用、环保等为解答的关键,侧重分析与应用能力的考查,注意化学与生活、环境的关系,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.决定物质性质的重要因素是物质结构.请回答下列问题.

(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
A通常显+3价,B元素的核外电子排布式为1s22s22p63s2.
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),已知3种离子晶体的晶格能数据如表:
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是TiN>MgO>CaO>KCl. 其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有12个.
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是CrO2.
(4)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A.离子键 B.极性键 C.金属键 D.配位键 E.氢键 F.非极性键.

(1)已知A和B为第三周期元素,其原子的第一至第四电离能如表所示:
| 电离能/kJ•mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图1所示),已知3种离子晶体的晶格能数据如表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是CrO2.
(4)某配合物的分子结构如图2所示,其分子内不含有AC(填序号).
A.离子键 B.极性键 C.金属键 D.配位键 E.氢键 F.非极性键.
1.下列说法中错误的是( )
| A. | 磺化、硝化、水化、风化、钝化等都是化学变化 | |
| B. | 干馏、常压分馏、减压分馏都是物理变化 | |
| C. | 甘油不是油,纯碱不是碱,酚醛树脂不是酯,干冰不是冰 | |
| D. | 水煤气、裂解气、焦炉气、天然气都是混合物 |
8.下列物质中,只含有共价键的是( )
| A. | Na2O | B. | NaCl | C. | HCl | D. | NaOH |
5.下列实验操作正确的是( )
| A. | 实验室制备肥皂,利用花生油与稀硫酸混合液在小烧杯中加热,直到油滴消失 | |
| B. | 配置菲林试剂,在硫酸铜溶液中加入少量的氢氧化钠溶液 | |
| C. | 检验卤代烃消去反应的有机产物:1-溴丙烷和NaOH的乙醇溶液混合后加热,将产生的蒸汽直接通入酸性高锰酸钾溶液,观察是否褪色 | |
| D. | 鉴别汽油和植物油:向汽油和植物油中分别加入一定量NaOH溶液加热振荡,观察油层是否消失或变薄 |
3.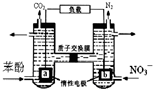 我国科学家构建了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐.下列说法正确的是:( )
我国科学家构建了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐.下列说法正确的是:( )
 我国科学家构建了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐.下列说法正确的是:( )
我国科学家构建了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时消除酸性废水中的硝酸盐.下列说法正确的是:( )| A. | a为正极 | |
| B. | 若右池产生0.672L气体(标况下),则转移电子0.15mol | |
| C. | 左池电极反应式为C6H6O+11H2O-28e-═6CO2↑+28H+ | |
| D. | 左池消耗的苯酚与右池消耗的NO3-的物质的量之比为28:5 |
 原电池是利用两个电极之间金属性的不同,产生电势差,从而使电子的流动,产生电流.随着科学技术的不断发展,以原电池原料为基础,科学家们研制出了各式各样的化学电源,请应用原电池相关知识回答:
原电池是利用两个电极之间金属性的不同,产生电势差,从而使电子的流动,产生电流.随着科学技术的不断发展,以原电池原料为基础,科学家们研制出了各式各样的化学电源,请应用原电池相关知识回答: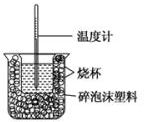 已知在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热.现利用如图装置进行中和热的测定,请回答下列问题:
已知在稀溶液中,酸跟碱发生中和反应生成1mol水时的反应热叫做中和热.现利用如图装置进行中和热的测定,请回答下列问题: