题目内容
将0.1mol?L-1的下列物质的水溶液,从常温加热到80℃,溶液的pH几乎不变的( )
| A、氯化钾 | B、氢氧化钠 |
| C、硫酸 | D、水 |
考点:pH的简单计算,水的电离
专题:电离平衡与溶液的pH专题
分析:水的电离是吸热反应,升高温度促进水电离,从常温加热到80℃,溶液的pH几乎不变,说明溶液中氢离子浓度变化不大,据此分析解答.
解答:
解:水的电离是吸热反应,升高温度促进水电离,从常温加热到80℃,溶液的pH几乎不变,说明溶液中氢离子浓度变化不大,
A.KCl是强酸强碱盐,其水溶液呈中性,升高温度促进水电离,溶液中氢离子浓度增大较明显,所以pH变化较明显,故A不选;
B.NaOH是强碱,在水溶液里完全电离,升高温度,促进水电离,水的离子积常数增大,溶液中NaOH电离出的氢氧根离子浓度远远大于水电离出氢氧根离子浓度,所以溶液中氢氧根离子浓度几乎不变,则溶液中氢离子浓度增大,溶液的pH增大,故B不选;
C.硫酸是强酸,在水溶液里完全电离生成氢离子和硫酸根离子,升高温度促进水电离,但硫酸电离出的氢离子浓度远远大于水电离出的氢离子浓度,所以溶液中氢离子浓度几乎不变,则溶液的pH几乎不变,故C选;
D.水的电离是吸热反应,升高温度促进水电离,溶液中氢离子浓度增大较明显,所以溶液pH变化较明显,故D不选;
故选C.
A.KCl是强酸强碱盐,其水溶液呈中性,升高温度促进水电离,溶液中氢离子浓度增大较明显,所以pH变化较明显,故A不选;
B.NaOH是强碱,在水溶液里完全电离,升高温度,促进水电离,水的离子积常数增大,溶液中NaOH电离出的氢氧根离子浓度远远大于水电离出氢氧根离子浓度,所以溶液中氢氧根离子浓度几乎不变,则溶液中氢离子浓度增大,溶液的pH增大,故B不选;
C.硫酸是强酸,在水溶液里完全电离生成氢离子和硫酸根离子,升高温度促进水电离,但硫酸电离出的氢离子浓度远远大于水电离出的氢离子浓度,所以溶液中氢离子浓度几乎不变,则溶液的pH几乎不变,故C选;
D.水的电离是吸热反应,升高温度促进水电离,溶液中氢离子浓度增大较明显,所以溶液pH变化较明显,故D不选;
故选C.
点评:本题考查溶液pH的计算,明确溶液中氢离子、氢氧根离子浓度变化是解本题关键,注意升高温度促进水电离但水的电离程度较小,为易错点.

练习册系列答案
相关题目
根据图,下列判断中正确的是( )
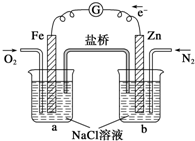

| A、烧杯a中的溶液pH降低 |
| B、烧杯b中发生氧化反应 |
| C、烧杯a中发生的反应为2H++2e-═H2 |
| D、烧杯b中发生的反应为2Cl--2e-═Cl2 |
下列有关化学用语表示正确的是( )
| A、二氧化硅的分子式 SiO2 | ||
B、质子数为53,中子数为78的碘原子:
| ||
| C、2-甲基-1-丁醇的结构简式:(CH3)2CHCH2CH2OH | ||
D、次氯酸的电子式  |
下列漂白剂不能使指示剂褪色的是( )
| A、次氯酸 | B、二氧化硫 |
| C、过氧化钠 | D、双氧水 |
用NA表示阿伏加德罗常数.下列说法中,正确的是( )
| A、1.8g重水(D2O)中含有的质子数为1.0 NA |
| B、500℃、30MPa下:N2(g)+3H2(g)?2NH3(g);△H=-38.6kJ?mol-1;将1.5NA的H2和过量N2在此条件下充分反应,放出热量19.3kJ |
| C、标准状况下,11.2 L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA |
| D、60 g石英晶体中含有的Si-O键数目为2NA |
 下表是元素周期表前三周期的一部分,按要求作答:
下表是元素周期表前三周期的一部分,按要求作答:
