题目内容
下列漂白剂不能使指示剂褪色的是( )
| A、次氯酸 | B、二氧化硫 |
| C、过氧化钠 | D、双氧水 |
考点:二氧化硫的化学性质
专题:
分析:A.HClO强氧化性漂白;
B.二氧化硫只能漂白有机色素,不能漂白指示剂;
C.过氧化钠强氧化性漂白;
D.双氧水强氧化性漂白.
B.二氧化硫只能漂白有机色素,不能漂白指示剂;
C.过氧化钠强氧化性漂白;
D.双氧水强氧化性漂白.
解答:
解:A.HClO强氧化性漂白,使指示剂褪色,故A不选;
B.二氧化硫只能漂白有机色素,不能漂白指示剂,故B选;
C.过氧化钠,具有强氧化性,能用作漂白剂,可使指示剂褪色,故C不选;
D.双氧水具有强氧化性,能用作漂白剂,可使指示剂褪色,故D不选.
故选B.
B.二氧化硫只能漂白有机色素,不能漂白指示剂,故B选;
C.过氧化钠,具有强氧化性,能用作漂白剂,可使指示剂褪色,故C不选;
D.双氧水具有强氧化性,能用作漂白剂,可使指示剂褪色,故D不选.
故选B.
点评:本题考查物质的漂白性,为高频考点,把握漂白原理为解答的关键,注意二氧化硫漂白性原理即可解答,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
1g氢气在氧气中完全燃烧生成液态水,放出142.9kJ热量,表示该反应的热化学方程式的是( )
A、H2(g)+
| ||
B、H2(g)+
| ||
| C、2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ/mol | ||
D、H2+
|
将0.1mol?L-1的下列物质的水溶液,从常温加热到80℃,溶液的pH几乎不变的( )
| A、氯化钾 | B、氢氧化钠 |
| C、硫酸 | D、水 |
短周期主族元素X、Y、Z、W在元素周期表中的位置关系如图,下列推论合理的是( )
| X | Y |
| W | Z |
| A、若Z的核电荷数是Y的两倍,则X为碳元素 |
| B、若W的核电荷数是Y的两倍,则X是氮元素 |
| C、原子半径:Z>Y>X |
| D、最简单氢化物的稳定性:Y>X>W |
下列说法正确的是( )
A、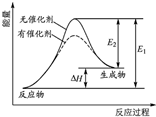 某反应的反应过程中能量变化如图所示,由如图分析可知催化剂不改变反应的焓变 | ||||||||||
| B、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | ||||||||||
C、已知:
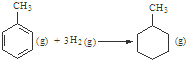 的△H为-384 kJ?mol-1 的△H为-384 kJ?mol-1 | ||||||||||
| D、常温下在0.10 mol?L-1的氨水中加入少量NH4Cl晶体,NH3?H2O的电离程度和溶液的pH均减小 |
NA代表阿伏加德罗常数的数值.下列说法中正确的是( )
| A、在1L0.1mol/L碳酸钠溶液中,阴离子总数大于0.1 NA |
| B、1molCaC2中含有阴离子数目为2NA |
| C、120gNaHSO4在水溶液和熔融状态下电离出来的离子总数均为3NA |
| D、2mol SO2和1 mol O2混合气体在V2O5存在的条件下于密闭容器中加热反应后容器内物质分子数小于2NA |