题目内容
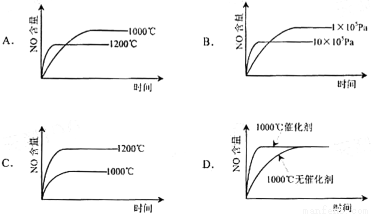
17.下列事实不能用电化学理论解释的是( )| A. | 轮船水线以下的船壳上装上一定数量的锌块 | |
| B. | 银质奖章久置后表面变暗 | |
| C. | 黄铜(铜锌合金)制作的铜锣不易产生铜绿 | |
| D. | 纯锌与稀H2SO4反应滴入少量的CuSO4溶液后反应速率加快 |
分析 根据是否能构成原电池判断,如果金属能构成原电池的就能产生电化学腐蚀,否则不能产生电化学腐蚀,据此分析解答.
解答 解:A、锌比铁活泼,锌被腐蚀而铁被保护,属于牺牲阳极的阴极保护法,可用原电池理论解释,故A错误;
B、银质奖牌长期放置后在其奖牌的表面变暗是由于金属银和空气中的成分发生反应的结果,属于化学腐蚀,与电化学腐蚀无关,故B正确;
C、黄铜(铜锌合金)制作的铜锣不易产生铜绿,锌被腐蚀而铜被保护,属于牺牲阳极的阴极保护法,可用原电池理论解释,故C错误;
D、滴入少量硫酸铜溶液后,锌把铜置换出来形成原电池反应,故加快反应速率,可用原电池原理解释,故D错误.
故选B.
点评 本题考查了金属的电化学腐蚀与防护,注意能用原电池理论和电解理论来解释的都属于电化学理论.

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
8. 被誉为中国“新四大发明’,的复方篙甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得)一泛认可的中国原创药品.截至2005年底,己被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青篙素(是一种由青篙中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明’,的复方篙甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得)一泛认可的中国原创药品.截至2005年底,己被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青篙素(是一种由青篙中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
 被誉为中国“新四大发明’,的复方篙甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得)一泛认可的中国原创药品.截至2005年底,己被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青篙素(是一种由青篙中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )
被誉为中国“新四大发明’,的复方篙甲醚是第一个由中国发现的全新化学结构的药品,也是目前在国际上获得)一泛认可的中国原创药品.截至2005年底,己被26个亚非国家指定为疟疾治疗一线用药,它在疟疾这一高传染性疾病治疗史上具有里程碑意义.其主要成分是青篙素(是一种由青篙中分离得到的具有新型化学结构的抗疟药),结构如图所示.有关该化合物的叙述正确的是( )| A. | 分子式为:C16H20O5 | |
| B. | 该化合物在一定条件下不能与NaOH溶液反应 | |
| C. | 青篙素与维生素一样是水溶性的 | |
| D. | 该化合物中含有过氧键,一定条件下有氧化性 |
9.下列离子方程式与所述事实相符且正确的是( )
| A. | 磁性氧化铁溶于稀硝酸:Fe3O4+8H++NO3-═3Fe3++NO↑+4H2O | |
| B. | Ca(HCO3)2溶液中加入过量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O | |
| C. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-═BaSO4↓+H2O |
6.用NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,22.4L乙醇完全燃烧后生成CO2的分子数为2NA | |
| B. | 56g的铁发生氧化还原反应,一定失去3NA个电子 | |
| C. | 标准状况下,22.4L氧气和二氧化碳混合气体中所含氧原子数为2NA | |
| D. | 0.1mol/L稀硫酸中含有SO42-离子数为0.1NA |
2.下列关于物质及其用途的关联中不正确的是( )
| A. | 乙醇-燃料 | B. | 蛋白质-生产葡萄糖 | ||
| C. | 淀粉-酿酒 | D. | 油脂-制造肥皂 |
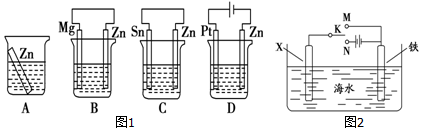
 4NO(g)+6H2O(g) △H=-1 025kJ/mol,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是( )
4NO(g)+6H2O(g) △H=-1 025kJ/mol,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是( )