题目内容
对于0.1mol?L-1 Na2CO3溶液,正确的是( )
| A、略升高温度,溶液的pH值增大 |
| B、2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
| C、c(Na+)+c(H+)=2 c(CO32-)+2c(HCO3-)+c(OH-) |
| D、加入少量NaOH固体,c(CO32-)与c(Na+)均增大 |
考点:盐类水解的应用
专题:盐类的水解专题
分析:A.升高温度促进碳酸钠水解;
B.溶液中存在物料守恒,根据物料守恒判断;
C.溶液中存在电荷守恒,根据电荷守恒判断;
D.加入少量NaOH固体,抑制碳酸钠水解.
B.溶液中存在物料守恒,根据物料守恒判断;
C.溶液中存在电荷守恒,根据电荷守恒判断;
D.加入少量NaOH固体,抑制碳酸钠水解.
解答:
解:A.碳酸钠水解是吸热反应,升高温度促进碳酸钠水解,溶液中氢氧根离子浓度增大,则溶液的PH增大,故A正确;
B.根据物料守恒得c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B错误;
C.根据电荷守恒得c(Na+)+c(H+)=2 c(CO32-)+c(HCO3-)+c(OH-),故C错误;
D.加入少量NaOH固体,氢氧根离子浓度增大抑制碳酸钠水解,NaOH能电离出钠离子,所以c(CO32-)与c(Na+)均增大,故D正确;
故选AD.
B.根据物料守恒得c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故B错误;
C.根据电荷守恒得c(Na+)+c(H+)=2 c(CO32-)+c(HCO3-)+c(OH-),故C错误;
D.加入少量NaOH固体,氢氧根离子浓度增大抑制碳酸钠水解,NaOH能电离出钠离子,所以c(CO32-)与c(Na+)均增大,故D正确;
故选AD.
点评:本题以碳酸钠为载体考查了盐类水解,根据盐类水解的影响因素结合电荷守恒和物料守恒来分析解答,易错选项是D,注意虽然钠离子不水解,但氢氧化钠会电离出钠离子,导致溶液中钠离子浓度增大,为易错点.

练习册系列答案
相关题目
X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、2s22p3和2s22p4,由这三种元素组成的常见化合物的化学式为( )
| A、X2YZ3 |
| B、X2YZ4 |
| C、XYZ4 |
| D、XYZ3 |
 按如图装置进行实验,下列描述正确的是(N装置中两个电极均为石墨棒)( )
按如图装置进行实验,下列描述正确的是(N装置中两个电极均为石墨棒)( )| A、Zn和C2上均发生氧化反应 |
| B、M 装置中SO42-移向Cu电极 |
| C、工作一段时间后装置M 中溶液pH变大,装置N中溶液pH变小 |
| D、Cu电极与C2电极上的电极反应相同 |
 某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )
某小组为研究电化学原理,设计如图装置.下列叙述不正确的是( )| A、a和b不连接时,铁片上会有金属铜析出 |
| B、a和b用导线连接时,铜片上发生的反应为:Cu2++2e-=Cu |
| C、无论a和b是否连接,铁片均会溶解,溶液从蓝色逐渐变成浅绿色 |
| D、a和b用导线连接时,可形成原电池,其中阳离子向负极移动 |
将足量CO2通入下列各溶液中,所含离子还能大量共存的是( )
| A、K+、SiO32-、NO3- |
| B、NH4+、Al3+、SO42- |
| C、Na+、OH-、SO42- |
| D、Na+、CH3COO-、ClO- |
化学用语是学习化学的重要工具.下列用来表示物质变化的化学用语正确的是( )
| A、0.5mol/L氢氧化钙溶液和0.5mol/L碳酸氢镁溶液等体积混合反应:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| B、少量的SO2通入Ca(ClO)2溶液中反应的离子方程式为:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO |
| C、将11.2L标准状况下的氯气通入200mL 2mol/L的FeBr2溶液中,离子反应方程式为:2Fe2++8Br-+5Cl2═2Fe3++4Br2+10Cl- |
| D、某锂电池电极总反应为:4Li+2SOCl2=4LiCl+S+SO2↑,则正极反应为:2SOCl2+4e-=4Cl-+S+SO2↑ |

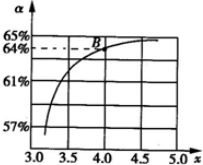

 在密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇:
在密闭容器中充有10mol CO与20mol H2,在催化剂作用下反应生成甲醇: