题目内容
3.(1)下列变化:①碘的升华;②氧气溶于水;③氯化钠溶于水;④烧碱熔化;⑤氯化氢溶于水;⑥氯化铵受热分解.(填序号)化学键没有被破坏的是①②;仅发生离子键破坏的是③④;仅发生共价键破坏的是⑤;既发生离子键又发生共价键破坏的是⑥.
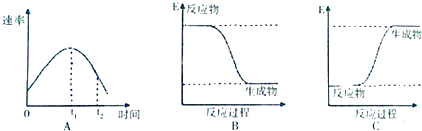
(2)某小组同学在烧杯中加入5 mL1.0 mol•L-1盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,如图A所示,该反应是放热(填“吸热”或“放热”)反应,其能量变化可用图中的B(填“B”或“C”)表示.
(3)已知拆开1 molH-H键、1 molN=N、1molN-H键分别需要吸收的能量为436kJ、946kJ、39lkJ.当1molNH3分解需要吸收(填“放出”或“吸收”)46KJ的热量.
分析 (1)先判断化学键是否被破坏,然后根据题意选择选项.化学键被破坏的情况有:发生化学反应、电解质的电离等;
(2)浓度越小,反应速率越小,温度越高,速率越大;放热反应中,反应物的总能量大于生成物的总能量,吸热反应中,反应物的总能量小于生成物的总能量;结合金属与酸的反应为放热反应分析;
(3)化学反应中,化学键断裂吸收能量,形成新化学键放出能量,根据方程式计算焓变=反应物总键能-生成物的总键能,以此计算反应热并判断吸热还是放热.
解答 解:(1)①碘的升华属于物理变化,只是状态发生变化,没有化学键的破坏;
②氧气溶于水,属于物理变化,没有化学键的破坏;
③氯化钠溶于水,在水分子的作用下,氯化钠中的离子键被破坏,所以破坏的是离子键;
④烧碱熔化中存在离子键,融化烧碱时,阴阳离子间的化学键被破坏,所以破坏的是离子键;
⑤氯化氢溶于水,在水分子的作用下,氯化氢中的共价键被破坏,所以破坏的是共价键;
⑥氯化铵受热分解,氯化铵是离子化合物,存在的化学键有离子键、共价键,受热分解时,阴阳离子间的化学键、及铵根离子中的共价键被破坏,所以破坏的是离子键、共价键;
故答案为:①②;③④;⑤;⑥;
(2)在烧杯中加入5mL 1.0mol/L盐酸,再放入用砂纸打磨过的铝条,观察产生H2的速率,开始时盐酸的浓度减小,速率应减小,但实际上增大,说明温度对速率的影响大于浓度对速率的影响,则该反应放热;放热反应中,反应物的总能量大于生成物的总能量,则图象B正确,
故答案为:放热;B;
(3)在反应2NH3?N2+3H2中,断裂2mol NH3,共形成6mol N-H键,吸收的能量为:6×391kJ=2346kJ,生成3mol H-H键,1mol N≡N键共放出的能量为:3×436kJ+946kJ=2254kJ,吸收的能量多,放出的能量少,该反应为吸热反应,吸收的热量为:2346kJ-2254kJ=92kJ,所以当1molNH3分解吸收热量为46KJ;
故答案为:吸收;46.
点评 本题考查化学反应与能量变化,为高频考点,侧重于学生的分析能力的考查,主要把握反应的特点,解题的关键是分析实验的过程,并结合题中所给的信息结合所学相关知识对问题进行探讨与分析,题目难度中等.

| A. | 非金属元素构成的单质中一定存在共价键 | |
| B. | 由不同种原子间形成的共价键不一定是极性键 | |
| C. | 含有共价键的化合物不一定是共价化合物 | |
| D. | 化学键断裂,不一定发生化学变化 |
| 浓 时间 度 温度 | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 1 | 800℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 800℃ | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 820℃ | 1.0 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
(1)在实验1中,反应在10至20min时间内,反应物A的平均速率为0.013mol/(L•min).
(2)在实验2中,A的初始浓度C2=1.0mol/L,反应经20minA的浓度就不再发生变化,进而可推测实验2中隐含的条件是加入了催化剂.
(3)在实验3中,A的初始浓度C3>1.0mol/L(填>、=、<).
(4)比较实验4和实验1,可推测该反应是吸热反应(选填“吸热”、“放热”).理由是升高温度,A的平衡浓度减小,说明升高温度平衡向正反应方向移动,故正反应是吸热反应.
| A. | 1-甲基戊烷 | B. | 2-乙基戊烷 | ||
| C. | 2,5-二甲基己烷 | D. | 2,4,4-三甲基戊烷 |
| A. | 水在结冰时体积膨胀,是由于水分子之间存在氢键 | |
| B. | NH3的稳定性很强,是因为其分子间能形成氢键 | |
| C. | 在氨水中水分子和氨分子之间也存在着氢键 | |
| D. | 分子间作用力较弱,破坏它所需能量较少 |
| A. | 向Al2(S04)3溶液中加入过量氨水:Al3++4NH3.H2O=AlO2-+4NH4++2H2O | |
| B. | 澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- | |
| C. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++N03-=3Fe3++NO↑+2H2O | |
| D. | 碱性锌锰电池正极反应:2MnO2+2H2O+2e一=2MnOOH+2OH- |
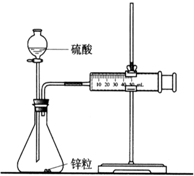 某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.
某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.