题目内容
12.在含2mol NaOH、1mol Na2SiO3的溶液中滴加稀盐酸至过量,下列关于沉淀质量(m)与盐酸体积(V)之间关系的图象正确的是( )| A. | 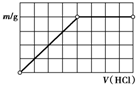 | B. | 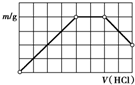 | C. | 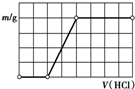 | D. | 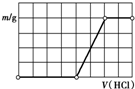 |
分析 在含2mol NaOH、1mol Na2SiO3的溶液中滴加稀盐酸至过量,在滴加过程中,HCl先和NaOH反应生成NaCl和水,然后再和Na2SiO3反应生成H2SiO3沉淀和NaCl,所以看到的现象是先没有沉淀生成后生成沉淀.
解答 解:在含2mol NaOH、1mol Na2SiO3的溶液中滴加稀盐酸至过量,在滴加过程中,HCl先和NaOH反应生成NaCl和水,然后再和Na2SiO3反应生成H2SiO3沉淀和NaCl,所以看到的现象是先没有沉淀生成后生成沉淀,
反应方程式分别为NaOH+HCl=NaCl+H2O、Na2SiO3+2HCl=H2SiO3↓+2NaCl,
根据方程式知,2molNaOH、1mol Na2SiO3都消耗2mol盐酸,故选C.
点评 本题考查化学方程式有关计算,为高频考点,把握物质性质及各个物理量之间的关系式是解本题关键,侧重考查学生分析判断能力,注意物质反应先后顺序,题目难度不大.

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
18.膳食纤维具有的突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图所示.下列有关芥子醇的说法正确的是( )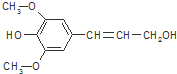

| A. | 芥子醇的分子式为C11H14O4,属于芳香族化合物 | |
| B. | 芥子醇分子中含9种不同化学环境的H原子 | |
| C. | 芥子醇分子中所有碳原子可能在同一平面上 | |
| D. | 1mol芥子醇能与足量溴水反应消耗3molBr2 |
3.下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A. | 稀硝酸和过量的铁屑反应:Fe+4H++NO3-═Fe3++NO↑+2H2O | |
| B. | 碳酸钠溶液水解的离子方程式:CO32-+2H2O?H2CO3+2OH- | |
| C. | 氢气的燃烧热为285.8 kJ/mol,则表示氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ/mol | |
| D. | 浓盐酸与MnO2共热制氯气:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O |
20.对于某些离子的检验及结论一定正确的是( )
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 某物质做焰色反应时,火焰呈黄色,则该物质中肯定不存在钾元素 | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
1.下列除去物质中的杂质(括号内为杂质)的方法,正确的是( )
| A. | 甲苯(苯酚):氢氧化钠,蒸馏 | B. | 乙酸丁酯(乙酸):碳酸钠,分液 | ||
| C. | 乙醇(苯酚):氢氧化钠,分液 | D. | 乙醇(乙酸):碱石灰,分液 |
2.设NA 为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1molN2与足量的H2反应,转移的电子数是0.6NA | |
| B. | 0.1 mol羟基( )中含有的电子数为0.7 NA )中含有的电子数为0.7 NA | |
| C. | 0.1 mol•L-1 MgCl2溶液中含有的Mg2+数目一定小于0.1 NA | |
| D. | 在精炼铜或电镀铜的过程中,当阴极析出铜32g,转移电子数均为NA |
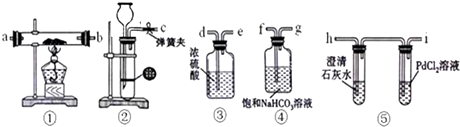
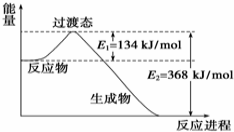 (1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是放热(填“吸热”或“放热”)反应,NO2和CO的总能量大于(填“大于”、“小于”或“等于”)CO2和NO的总能量.
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是放热(填“吸热”或“放热”)反应,NO2和CO的总能量大于(填“大于”、“小于”或“等于”)CO2和NO的总能量.