题目内容
1.下列除去物质中的杂质(括号内为杂质)的方法,正确的是( )| A. | 甲苯(苯酚):氢氧化钠,蒸馏 | B. | 乙酸丁酯(乙酸):碳酸钠,分液 | ||
| C. | 乙醇(苯酚):氢氧化钠,分液 | D. | 乙醇(乙酸):碱石灰,分液 |
分析 A.甲苯不溶于水,可分液分离;
B.乙酸丁酯不溶于饱和碳酸钠溶液,可分液;
C.乙醇溶于水;
D.乙酸与碱石灰反应生成盐,可增大混合物的沸点差.
解答 解:A.甲苯不溶于水,苯酚与氢氧化钠溶液反应,溶液分层,可分液分离,故A错误;
B.乙酸丁酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应,可分液,故B正确;
C.乙醇溶于水,苯酚与氢氧化钠反应生成溶于水的苯酚钠,不能分液,故C错误;
D.乙酸与碱石灰反应生成盐,可增大混合物的沸点差,应用蒸馏的方法分离,故D错误.
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、发生的反应及混合物分离方法选择为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识与实验相结合,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
9.已知短周期元素的离子:aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子序数 d>c>b>a | B. | 原子半径 A>B>D>C | ||
| C. | 离子半径 C2->D->B+>A2+ | D. | 阴离子的还原性C2-<D- |
16.下列转化必须加入氧化剂才能进行的是( )
| A. | HCO3-→CO2 | B. | MnO4-→Mn2+ | C. | Fe2+→Fe3+ | D. | Na2O2→O2 |
11.如图是一种航天器能量储存系统原理示意图.下列说法正确的是 ( )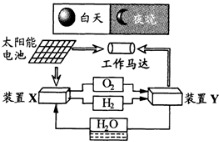

| A. | 装置X能实现燃料电池的燃料和氧化剂再生 | |
| B. | 装置Y中负极的电极反应式为:O2+2H2O+4e-=4OH- | |
| C. | 装置X是原电池,装置Y是电解池 | |
| D. | 装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |