题目内容
8.Y为短周期元素,若其最高价氧化物对应水化物的化学式为HYO4,则此时Y元素的化合价为+7,Y原子的最外层电子数为7,其气态氢化物与其中间价态的氧化物反应的化学方程式为2ClO2+8HCl=5Cl2+4H2O.分析 Y为短周期元素,若其最高价氧化物对应水化物的化学式为HYO4,则Y为Cl元素;根据化合物中元素化合价的代数和为零计算;Y元素的最高正价等于最外层电子数;HCl与ClO2反应生成氯气和水.
解答 解:Y为短周期元素,若其最高价氧化物对应水化物的化学式为HYO4,则Y为Cl元素;由化合物中元素化合价的代数和为零可知,Cl元素的化合价为+7价;Cl元素的最高正价等于最外层电子数,则原子的最外层电子数为7;HCl与ClO2反应生成氯气和水,其反应方程式为:2ClO2+8HCl=5Cl2+4H2O;
故答案为:+7;7;2ClO2+8HCl=5Cl2+4H2O.
点评 本题考查了元素周期表的结构与应用,题目难度不大,注意把握主族元素的最高正化合价与最外层电子数的关系,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
18.W、X、Y、Z均为短周期主族元素,原子序数依次增大.W的最外层电子数、电子层数和主族序数均相等.Y原子最外层电子数与W、X原子最外层电子数之和相等.X原子的最外层电子数是内层电子数的2倍还多1个.Z是所在周期中主族元素原子半径最大的元素.下列说法正确的是( )
| A. | 离子半径大小顺序为:Z>X>Y>W | |
| B. | W、X、Y三种元素都属于非金属元素,它们之间只能形成共价化合物 | |
| C. | X、Y、Z三种元素与W 元素形成的最简单化合物的沸点依次升高 | |
| D. | X、Y、Z三种元素形成的化合物的水溶液一定显中性 |
19.根据等电子原理,下列各组分子或离子的空间构型不相似的是( )
| A. | NH4+和CH4 | B. | H3O+和NH3 | C. | NO3-和CO32- | D. | CO2和H2O |
13.下列制质中,酸性由强到弱错误的是( )
| A. | HClO4 H2SO4 H3PO4 H4SiO4 | B. | H2SO4 H2SO3 HNO3 HNO2 | ||
| C. | HClO4 HClO3 HClO2 HClO | D. | HClO4 H2SO4 H2SO3 H2CO3 |
20.向新制氯水中加入少量下列物质,能增强溶液漂白能力的是( )
| A. | 碳酸钙粉末 | B. | 稀硫酸 | C. | 氯化钙溶液 | D. | 二氧化硫水溶液 |
12.在100mL H2SO4与CuSO4的混合液中,用石墨作电极电解,两极上均收集到2.24L气体(标准状况),则原混合溶液中Cu2+的物质的量浓度为( )
| A. | 0.5 mol/L | B. | 1 mol/L | C. | 3 mol/L | D. | 4 mol/L |
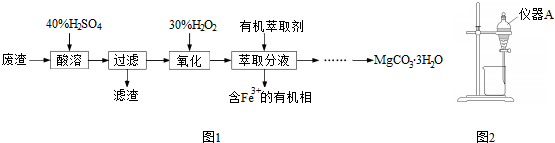
 ,B
,B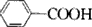 ,CCH2(NH2)COOH.
,CCH2(NH2)COOH.