题目内容
下列生活中的做法不恰当的是( )
| A、贮氯罐意外泄漏,应沿逆风方向疏散群众 |
| B、铝制餐具不宜长期存放酸性、碱性或咸的食物 |
| C、氢氧化铝可作胃酸的中和剂 |
| D、漂白粉能在空气中长期存放 |
考点:氯气的物理性质,氯、溴、碘及其化合物的综合应用,铝的化学性质,两性氧化物和两性氢氧化物
专题:
分析:A、氯气有毒,且氯气会顺着风向流到,所以应该逆风向疏散人群;
B、金属铝可以和强酸以及强碱反应;
C、氢氧化铝为难溶物,能够中和胃酸中的盐酸;
D、漂白粉在空气中与二氧化碳反应生成次氯酸,次氯酸见光容易分解而导致变质.
B、金属铝可以和强酸以及强碱反应;
C、氢氧化铝为难溶物,能够中和胃酸中的盐酸;
D、漂白粉在空气中与二氧化碳反应生成次氯酸,次氯酸见光容易分解而导致变质.
解答:
解:A、氯气是一种有毒的气体,氯气会顺着风向流到,所以疏散时应该逆着风向转移,故A正确;
B、金属铝可以和强酸以及强碱反应,所以不可用铝制餐具长时间存放酸性或碱性食物,故B正确;
C、氢氧化铝能够与胃酸中的盐酸反应,能够作胃酸的中和剂,故C正确;
D、HClO虽是强氧化性的酸,但它是比碳酸还弱的酸,能与水和二氧化碳发生复分解反应,生成CaCO3和 HClO,故漂白粉不能长期在空气中放置,故D错误,故选D.
B、金属铝可以和强酸以及强碱反应,所以不可用铝制餐具长时间存放酸性或碱性食物,故B正确;
C、氢氧化铝能够与胃酸中的盐酸反应,能够作胃酸的中和剂,故C正确;
D、HClO虽是强氧化性的酸,但它是比碳酸还弱的酸,能与水和二氧化碳发生复分解反应,生成CaCO3和 HClO,故漂白粉不能长期在空气中放置,故D错误,故选D.
点评:本题主要考查的是生活中的化学,涉及氯气的物理性质、漂白粉的放置、铝以及氢氧化铝的两性,难度不大.

练习册系列答案
相关题目
若要制得CH3CH2Cl,最好的方法是( )
| A、CH3CH3与Cl2取代反应 |
| B、CH2=CH2与Cl2加成反应 |
| C、CH2=CH2与HCl加成反应 |
| D、CH3CH2Br与Cl2置换反应 |
城市空气质量日报不涉及的物质是( )
| A、SO2 |
| B、CO2 |
| C、氮的氧化物 |
| D、可吸入颗粒 |
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、1mol OH-含有的电子数目为9NA | ||
| B、1mol Cl2和氢氧化钠完全反应,转移的电子数目为NA | ||
| C、室温下,1L pH=1的H2SO4溶液中,由水电离出的H+数目为0.1NA | ||
D、1mol
|
如图是以石墨为电极,电解CuCl2溶液的装置图,下列说法正确的是( )
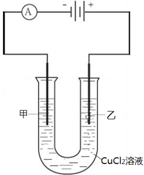

| A、甲电极为阳极 |
| B、阴极处能产生使湿润淀粉KI试纸变蓝的气体 |
| C、阴极发生还原反应 |
| D、通电时,溶液中的离子作定向运动 |
下列离子方程式正确的是( )
| A、钠和水的反应:Na+H2O=Na++OH-+H2↑ |
| B、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| D、氢氧化钡溶液跟稀硫酸反应:Ba2++OH-+H++SO42-=BaSO↓+H2O |
 高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂.
高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂.