题目内容
下列离子方程式正确的是( )
| A、钠和水的反应:Na+H2O=Na++OH-+H2↑ |
| B、氯化铝溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
| D、氢氧化钡溶液跟稀硫酸反应:Ba2++OH-+H++SO42-=BaSO↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.转移电子不守恒;
B.氢氧化铝难溶于弱碱但能溶于强碱;
C.稀硫酸具有弱氧化性,能将变价金属氧化为较低价态;
D.二者反应生成硫酸钡和水,但氢离子、氢氧根离子及水的离子积常数都是2.
B.氢氧化铝难溶于弱碱但能溶于强碱;
C.稀硫酸具有弱氧化性,能将变价金属氧化为较低价态;
D.二者反应生成硫酸钡和水,但氢离子、氢氧根离子及水的离子积常数都是2.
解答:
解:A.转移电子不守恒,离子方程式为2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.氢氧化铝难溶于弱碱但能溶于强碱,离子方程式为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B正确;
C.稀硫酸具有弱氧化性,能将变价金属氧化为较低价态,离子方程式为:Fe+2H+=Fe2++H2↑,故C错误;
D.二者反应生成硫酸钡和水,但氢离子、氢氧根离子及水的离子积常数都是2,离子方程式为Ba2++2OH-+2H++SO42-=BaSO↓+2H2O,故D错误;
故选B.
B.氢氧化铝难溶于弱碱但能溶于强碱,离子方程式为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故B正确;
C.稀硫酸具有弱氧化性,能将变价金属氧化为较低价态,离子方程式为:Fe+2H+=Fe2++H2↑,故C错误;
D.二者反应生成硫酸钡和水,但氢离子、氢氧根离子及水的离子积常数都是2,离子方程式为Ba2++2OH-+2H++SO42-=BaSO↓+2H2O,故D错误;
故选B.
点评:本题考查离子方程式正误判断,侧重考查氧化还原反应、复分解反应,明确物质性质及离子方程式书写规则即可解答,注意D中易漏掉部分离子反应,易错选项是C.

练习册系列答案
相关题目
下列生活中的做法不恰当的是( )
| A、贮氯罐意外泄漏,应沿逆风方向疏散群众 |
| B、铝制餐具不宜长期存放酸性、碱性或咸的食物 |
| C、氢氧化铝可作胃酸的中和剂 |
| D、漂白粉能在空气中长期存放 |
在密闭容器中进行如下反应:X2(g)+Y2(g)?2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A、Z为0.3mol/L |
| B、Y2为0.1mol/L |
| C、X2为0.2mol/L |
| D、Z为0.4mol/L |
下列化合物中,既含有离子键又含有共价键的是( )
| A、HBr |
| B、CO2 |
| C、CaCl2 |
| D、NaOH |
春节燃放烟花后的烟雾中常含有CO、CO2、SO2等气体,所以烟花燃烧后的烟雾属于( )
| A、氧化物 | B、化合物 |
| C、纯净物 | D、混合物 |
下列说法正确的是( )
A、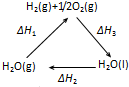 △H1=△H2+△H3 |
B、 在催化剂条件下,反应的活化能等于E1+E2 |
C、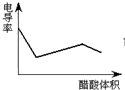 表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线 |
D、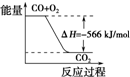 可表示由CO(g)生成CO2(g)的反应过程和能量关系 |

 是一种新型可生物降解的高分子材料,主要用于制造可降解纤维,可降解塑料和医用材料.它以淀粉为原料,先水解为葡萄糖,再在乳酸菌的作用下降葡萄糖转变为乳酸
是一种新型可生物降解的高分子材料,主要用于制造可降解纤维,可降解塑料和医用材料.它以淀粉为原料,先水解为葡萄糖,再在乳酸菌的作用下降葡萄糖转变为乳酸 ,乳酸在催化剂的催化下聚合成聚乳酸.聚乳酸材料废弃后,先水解成乳酸,乳酸在微生物的作用下分解为CO2和H2O.请用化学方程式表示上述聚合与降解的过程.
,乳酸在催化剂的催化下聚合成聚乳酸.聚乳酸材料废弃后,先水解成乳酸,乳酸在微生物的作用下分解为CO2和H2O.请用化学方程式表示上述聚合与降解的过程.