��Ŀ����
������ʵ�����г����Լ���Ҳ�ǹ�ҵ����Ҫԭ�ϣ�
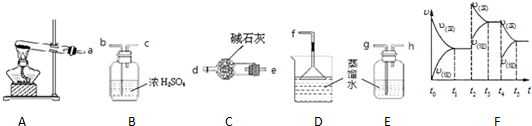
��1��ijѧϰС�����Ʊ������İ�ˮ����ѡ�õ��Լ��У���NH4Cl �ڣ�NH4��2CO3���ṩ��װ�����£���ش��������⣺
��װ��A�Թ��ڷ�����Ӧ�Ļ�ѧ����ʽΪ ��
�ڴ��ṩ��������ѡ����װһ�ױ�ʵ��ĺ��������װ�ã���������������˳��Ϊ����ͼ�б�ע�ĵ��ܿڷ��ű�ʾ��a�� ��
��2������������ȼ�գ�����ˮ��һ�ֵ��ʣ�
��֪��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ?mol-1
2H2��g��+O2��g���T2H2O��l����H=-572kJ?mol-1
д������������ȼ������Һ̬ˮ����̬���ʵ��Ȼ�ѧ����ʽ�� ��
��3����֪��һ�������£���1mol N2��3mol H2�����һ��10L���ܱ������з����ķ�ӦΪN2+3H2
2NH3��5min��ﵽƽ�⣬ƽ��ʱ�����������Ϊ25%��
�ٸ÷�Ӧ��ƽ�ⳣ������ʽK= ��
�ڴӷ�Ӧ��ʼ��ƽ��ʱ��N2�ķ�Ӧ����v��N2��= ��
��4����ҵ������������Ϊ��Ҫԭ����ȡ���ᣮ���ݻ��㶨���ܱ������н��з�Ӧ2NO��g��+O2��g��?2NO2��g����H��0���÷�Ӧ�ķ�Ӧ���ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ��ͼF��ʾ����t2��t4ʱ��ֻ�ı�һ������������˵����ȷ���ǣ���ѡ����ţ� ��
A����t1-t2ʱ�������������������ѹǿ���ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
B����t2ʱ����ȡ�Ĵ�ʩ�����������¶�
C����t3-t4ʱ��������������������ܶȱ��ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
D����t5ʱ��������NO2��������������������е����ֵ
��5��Ϊ���鰱�����ᷴӦ�õ���ij�ֳ������ʵijɷ֣�ijͬѧ����������ʵ�飺�ټ��ȵ�����Ʒ�������壬����һ��������ʹʪ��ĺ�ɫʯ����ֽ��������һ��������ʹ����ʯ��ˮ����ǣ���ȡ�����õ�����Ʒ����ˮ������������BaCl2��Һ��û�����Ա仯���ɴ˿�֪�õ��ʵ���Ҫ�ɷֿ����� ����ѡ����ţ���
A��NH4Cl B����NH4��2CO3 C��NH4HCO3 D��NH4NO3
��6�����᳧����Na2CO3��Һ���մ���β��NO2����CO2����9.2g NO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol����Ӧ�����ӷ���ʽ�� ��

��1��ijѧϰС�����Ʊ������İ�ˮ����ѡ�õ��Լ��У���NH4Cl �ڣ�NH4��2CO3���ṩ��װ�����£���ش��������⣺
��װ��A�Թ��ڷ�����Ӧ�Ļ�ѧ����ʽΪ
�ڴ��ṩ��������ѡ����װһ�ױ�ʵ��ĺ��������װ�ã���������������˳��Ϊ����ͼ�б�ע�ĵ��ܿڷ��ű�ʾ��a��
��2������������ȼ�գ�����ˮ��һ�ֵ��ʣ�
��֪��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ?mol-1
2H2��g��+O2��g���T2H2O��l����H=-572kJ?mol-1
д������������ȼ������Һ̬ˮ����̬���ʵ��Ȼ�ѧ����ʽ��
��3����֪��һ�������£���1mol N2��3mol H2�����һ��10L���ܱ������з����ķ�ӦΪN2+3H2
| ���� |
| ���¸�ѹ |
�ٸ÷�Ӧ��ƽ�ⳣ������ʽK=
�ڴӷ�Ӧ��ʼ��ƽ��ʱ��N2�ķ�Ӧ����v��N2��=
��4����ҵ������������Ϊ��Ҫԭ����ȡ���ᣮ���ݻ��㶨���ܱ������н��з�Ӧ2NO��g��+O2��g��?2NO2��g����H��0���÷�Ӧ�ķ�Ӧ���ʣ�v����ʱ�䣨t���仯�Ĺ�ϵ��ͼF��ʾ����t2��t4ʱ��ֻ�ı�һ������������˵����ȷ���ǣ���ѡ����ţ�
A����t1-t2ʱ�������������������ѹǿ���ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
B����t2ʱ����ȡ�Ĵ�ʩ�����������¶�
C����t3-t4ʱ��������������������ܶȱ��ֲ����жϷ�Ӧ�Ѵﵽƽ��״̬
D����t5ʱ��������NO2��������������������е����ֵ
��5��Ϊ���鰱�����ᷴӦ�õ���ij�ֳ������ʵijɷ֣�ijͬѧ����������ʵ�飺�ټ��ȵ�����Ʒ�������壬����һ��������ʹʪ��ĺ�ɫʯ����ֽ��������һ��������ʹ����ʯ��ˮ����ǣ���ȡ�����õ�����Ʒ����ˮ������������BaCl2��Һ��û�����Ա仯���ɴ˿�֪�õ��ʵ���Ҫ�ɷֿ�����
A��NH4Cl B����NH4��2CO3 C��NH4HCO3 D��NH4NO3
��6�����᳧����Na2CO3��Һ���մ���β��NO2����CO2����9.2g NO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol����Ӧ�����ӷ���ʽ��
���㣺������ȡ������,��ѧƽ�⽨���Ĺ���,��ѧƽ��ĵ�������
ר�⣺��ѧƽ��ר��,Ԫ�ؼ��仯����
��������1����̼��識��ȷֽ����ɰ�����������̼��ˮ��
��̼��立ֽ�����庬�ж�����̼��ͨ��ʢ�м�ʯ�ҵĸ���ܳ�ȥ������̼����ͨ��ˮ�У�������������ˮ��������������D���տ��Է�ֹ������
��2������֪����ʽ�������ø�˹���ɽ��
��3���ٻ�ѧƽ�ⳣ����ƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ��
����μӷ�Ӧ�ĵ��������ʵ������������η�������Ե����ʵ������ٸ�������������δ֪����Ȼ�����v=
���㷴Ӧ���ʣ�
��4��2NO��g��+O2��g��?2NO2��g������H��0���÷�Ӧ�����������С�����ȷ�Ӧ��
A��ѹǿ����˵����Ӧ�ﵽƽ�⣻
B����Ӧ�����ȷ�Ӧ�������淴Ӧ��������ƽ��������У�
C����Ӧ�����������غ㣬������䣬�������ܶȲ��䣻
D������ͼ���������NO2�����������t3��t4ʱ���
��5�����ȵ�����Ʒ�����������壬����һ��������ʹʪ��ĺ�ɫʯ����ֽ������������Ϊ������˵������笠����ӣ���һ��������ʹ����ʯ��ˮ����ǣ�˵��̼������ӻ�̼��������ӣ�ȡ�����õ�����Ʒ����ˮ������������BaCl2��Һ��û�����Ա仯��˵��û��̼��������ӣ��ɴ��Ƶ������ʵ���Ҫ�ɷ֣�
��6��9.2g NO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol����ÿ2mol NO2��Na2CO3��Һ��Ӧʱת�Ƶ���1mol�������ɵ����ᣬ���ݻ��ϼ۵ı仯�ж�������Դ���д��Ӧ�����ӷ���ʽ��
��̼��立ֽ�����庬�ж�����̼��ͨ��ʢ�м�ʯ�ҵĸ���ܳ�ȥ������̼����ͨ��ˮ�У�������������ˮ��������������D���տ��Է�ֹ������
��2������֪����ʽ�������ø�˹���ɽ��
��3���ٻ�ѧƽ�ⳣ����ƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ��
����μӷ�Ӧ�ĵ��������ʵ������������η�������Ե����ʵ������ٸ�������������δ֪����Ȼ�����v=
| ��C |
| ��t |
��4��2NO��g��+O2��g��?2NO2��g������H��0���÷�Ӧ�����������С�����ȷ�Ӧ��
A��ѹǿ����˵����Ӧ�ﵽƽ�⣻
B����Ӧ�����ȷ�Ӧ�������淴Ӧ��������ƽ��������У�
C����Ӧ�����������غ㣬������䣬�������ܶȲ��䣻
D������ͼ���������NO2�����������t3��t4ʱ���
��5�����ȵ�����Ʒ�����������壬����һ��������ʹʪ��ĺ�ɫʯ����ֽ������������Ϊ������˵������笠����ӣ���һ��������ʹ����ʯ��ˮ����ǣ�˵��̼������ӻ�̼��������ӣ�ȡ�����õ�����Ʒ����ˮ������������BaCl2��Һ��û�����Ա仯��˵��û��̼��������ӣ��ɴ��Ƶ������ʵ���Ҫ�ɷ֣�
��6��9.2g NO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol����ÿ2mol NO2��Na2CO3��Һ��Ӧʱת�Ƶ���1mol�������ɵ����ᣬ���ݻ��ϼ۵ı仯�ж�������Դ���д��Ӧ�����ӷ���ʽ��
���
�⣺��1��̼��立ֽ�ķ���ʽΪ����NH4��2CO3
2NH3��+CO2��+H2O���ʴ�Ϊ����NH4��2CO3
2NH3��+CO2��+H2O��
��̼��立ֽ�����庬�ж�����̼��ͨ��ʢ�м�ʯ�ҵĸ���ܳ�ȥ������̼����ͨ��ˮ�У�������������ˮ��������������D���տ��Է�ֹ������
�ʴ�Ϊ��e d f��
��2����N2��g��+3H2��g��?2NH3��g����H=-92.4kJ?mol-1
��2H2��g��+O2��g���T2H2O��l����H=-572kJ?mol-1
���ݸ�˹���ɢڡ�3-�١��ڵã�4NH3��g��+3O2��g��=2N2��g��+6H2O��l����H=-1531.2 kJ?mol-1 ��
�ʴ�Ϊ��4NH3��g��+3O2��g��=2N2��g��+6H2O��l����H=-1531.2 kJ?mol-1��
��3���ٸ÷�Ӧ��ƽ�ⳣ������ʽK=
���ʴ�Ϊ��K=
��
����μӷ�Ӧ�ĵ��������ʵ���xmol��
N2 +3H2
2NH3
��ʼ��mol����1 3 0
�仯��mol����x 3x 2x
ƽ�⣨mol����1-x 3-3x 2x
5min��ﵽƽ�⣬ƽ��ʱ�����������=
��100%=25%��
���x=0.4��
N2�ķ�Ӧ����v��N2��=
=
=0.008mol/��L�qmin����
�ʴ�Ϊ��0.008mol/��L�qmin����
��4��A���÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ�����º����������£�ѹǿ���䣬˵������ƽ�⣬��A��ȷ��
B������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�ƶ�����t2ʱ�����������ʶ�����������Ӧ����������࣬ƽ��������Ӧ�ƶ����÷�Ӧ����Ӧ�����������С�ķ�Ӧ������ѹǿƽ��������Ӧ���У�ת��������B��ȷ��
C�����������£���Ӧ�����������������䣬�ܶ�ʼ�ղ��䣬���Բ���˵����Ӧ�ﵽƽ��״̬����C����
D����ͼ��֪����t2ʱ���ı�����ƽ��������Ӧ�ƶ���t3ʱ����ƽ�⣬t4ʱ˲������Ӧ���ʲ��䣬�淴Ӧ���ʼ�С��ƽ��������Ӧ���У�Ӧ��NO2���͵�Ũ�ȣ���������NO2�����������t3ʱֵ�����D����
��ѡAB��
��5�����ȵ�����Ʒ�����������壬����һ��������ʹʪ��ĺ�ɫʯ����ֽ������������Ϊ������˵������笠����ӣ���һ��������ʹ����ʯ��ˮ����ǣ�˵��̼������ӻ�̼��������ӣ�ȡ�����õ�����Ʒ����ˮ������������BaCl2��Һ��û�����Ա仯��˵��û��̼��������ӣ�˵�����к���笠����Ӻ�̼������ӣ����Ե��ʵ���Ҫ�ɷ�NH4HCO3��
�ʴ�Ϊ��C��
��6��9.2gNO2�����ʵ���
=0.2mol����0.2molNO2��Na2CO3��Һ��ȫ��Ӧʱת�Ƶ���0.1mol����2molNO2��Na2CO3��Һ��Ӧʱת�Ƶ���1mol����N�Ļ��ϼ۷ֱ���+4�۱仯Ϊ+5�ۺ�+3�ۣ��ڼ�����Һ��Ӧ����NO3-��NO2-����Ӧ�����ӷ���ʽΪ��2NO2+CO32-=NO3-+NO2-+CO2��
�ʴ�Ϊ��2NO2+CO32-=NO3-+NO2-+CO2��
| ||
| ||
��̼��立ֽ�����庬�ж�����̼��ͨ��ʢ�м�ʯ�ҵĸ���ܳ�ȥ������̼����ͨ��ˮ�У�������������ˮ��������������D���տ��Է�ֹ������
�ʴ�Ϊ��e d f��
��2����N2��g��+3H2��g��?2NH3��g����H=-92.4kJ?mol-1
��2H2��g��+O2��g���T2H2O��l����H=-572kJ?mol-1
���ݸ�˹���ɢڡ�3-�١��ڵã�4NH3��g��+3O2��g��=2N2��g��+6H2O��l����H=-1531.2 kJ?mol-1 ��
�ʴ�Ϊ��4NH3��g��+3O2��g��=2N2��g��+6H2O��l����H=-1531.2 kJ?mol-1��
��3���ٸ÷�Ӧ��ƽ�ⳣ������ʽK=
| C2(NH3) |
| C(N2)C3(H2) |
| C2(NH3) |
| C(N2)C3(H2) |
����μӷ�Ӧ�ĵ��������ʵ���xmol��
N2 +3H2
| ���� |
| ���¸�ѹ |
��ʼ��mol����1 3 0
�仯��mol����x 3x 2x
ƽ�⣨mol����1-x 3-3x 2x
5min��ﵽƽ�⣬ƽ��ʱ�����������=
| 2x |
| 1-x+3-3x+2x |
���x=0.4��
N2�ķ�Ӧ����v��N2��=
| ��C(N2) |
| ��t |
| 0.4mol/10L |
| 5min |
�ʴ�Ϊ��0.008mol/��L�qmin����
��4��A���÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ�����º����������£�ѹǿ���䣬˵������ƽ�⣬��A��ȷ��
B������Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�ƶ�����t2ʱ�����������ʶ�����������Ӧ����������࣬ƽ��������Ӧ�ƶ����÷�Ӧ����Ӧ�����������С�ķ�Ӧ������ѹǿƽ��������Ӧ���У�ת��������B��ȷ��
C�����������£���Ӧ�����������������䣬�ܶ�ʼ�ղ��䣬���Բ���˵����Ӧ�ﵽƽ��״̬����C����
D����ͼ��֪����t2ʱ���ı�����ƽ��������Ӧ�ƶ���t3ʱ����ƽ�⣬t4ʱ˲������Ӧ���ʲ��䣬�淴Ӧ���ʼ�С��ƽ��������Ӧ���У�Ӧ��NO2���͵�Ũ�ȣ���������NO2�����������t3ʱֵ�����D����
��ѡAB��
��5�����ȵ�����Ʒ�����������壬����һ��������ʹʪ��ĺ�ɫʯ����ֽ������������Ϊ������˵������笠����ӣ���һ��������ʹ����ʯ��ˮ����ǣ�˵��̼������ӻ�̼��������ӣ�ȡ�����õ�����Ʒ����ˮ������������BaCl2��Һ��û�����Ա仯��˵��û��̼��������ӣ�˵�����к���笠����Ӻ�̼������ӣ����Ե��ʵ���Ҫ�ɷ�NH4HCO3��
�ʴ�Ϊ��C��
��6��9.2gNO2�����ʵ���
| 9.2g |
| 46g/mol |
�ʴ�Ϊ��2NO2+CO32-=NO3-+NO2-+CO2��
����������Ϊ�ۺ��壬�����˰������Ʊ������ʵļ��飬��˹������Ӧ�ȣ���ѧƽ����ƶ���ƽ��״̬���жϣ�������ԭ����ʽ����д����Ŀ�Ѷȴ���Ϥƽ��״̬��Ӱ�������ǽ���ؼ���

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
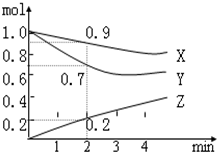 ij�¶�ʱ��2L������X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ����ͼ�����ݷ�����
ij�¶�ʱ��2L������X��Y��Z�������ʵ����ʵ�����ʱ��ı仯������ͼ��ʾ����ͼ�����ݷ�����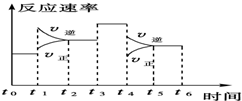 һ�ܷ���ϵ�з������з�Ӧ��N2+3H2?2NH3����H��0����ͼ��ijһʱ����з�Ӧ�����뷴Ӧ���̵����߹�ϵͼ���ش��������⣺
һ�ܷ���ϵ�з������з�Ӧ��N2+3H2?2NH3����H��0����ͼ��ijһʱ����з�Ӧ�����뷴Ӧ���̵����߹�ϵͼ���ش��������⣺