题目内容
已知BrFx与H2O按物质的量之比3:5反应的产物是HF、HBrO3、Br2、O2,BrFx中的x= ,该反应中的氧化剂是 ,还原剂是 .该反应中若有5molH2O全做还原剂,则其能还原BrFx的物质的量为 .
考点:氧化还原反应的计算,氧化还原反应
专题:氧化还原反应专题
分析:BrFx与H2O按物质的量之比3:5反应的产物是HF、HBrO3、Br2、O2,则反应为3BrFx+5H2O=9HF+HBrO3+Br2+O2,由F原子守恒可知,x=3,Br元素的化合价由+3价降低为0,Br元素的化合价以由+3价升高为+5价,O元素的化合价由-2价升高为0,以此计算解答.
解答:
解:BrFx与H2O按物质的量之比3:5反应的产物是HF、HBrO3、Br2、O2,则反应为3BrFx+5H2O=9HF+HBrO3+Br2+O2,由F原子守恒可知,x=3,Br元素的化合价由+3价降低为0,则氧化剂为BrF3,Br元素的化合价以由+3价升高为+5价,O元素的化合价由-2价升高为0,还原剂为BrF3、H2O,若有5molH2O全做还原剂,失去电子为5mol×2=10mol,由电子守恒可知,则其能还原BrFx的物质的量为
=
mol或3.3 mol,
故答案为:3;BrF3;BrF3、H2O;
mol或3.3 mol.
| 10mol |
| (3-0) |
| 10 |
| 3 |
故答案为:3;BrF3;BrF3、H2O;
| 10 |
| 3 |
点评:本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化及电子守恒计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
已知乙烯分子是平面结构,因此1,2-二氯乙烯可形成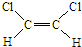 和
和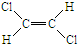 两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )
两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )
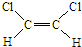 和
和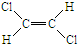 两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )
两种不同的空间异构体,称为顺反异构.下列能形成类似上述空间异构体的是( )| A、1-丁烯 | B、2-甲基-1-丙烯 |
| C、2-丁烯 | D、丁烷 |