题目内容
5.已知反应:①3Cl2+6NaOH=5NaCl+NaClO3+3H2O;②H2SO4(浓)+H2S=SO2↑+S↓+2H2O;③4HCl+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑=2H2O.试回答:(1)反应①中氧化剂与还原剂的质量之比为5:1.
(2)用单线桥标出反应②中电子得失(标在原化学方程式上).
(3)反应③中被氧化的Cl-的个数之比为1:1.
(4)试配平下列化学方程式:2MnO${\;}_{4}^{-}$+10Cl-+16H+=2Mn2++5Cl2+8H2O.
分析 (1)反应①中只有Cl元素化合价发生变化;
(2)H2S+H2SO4(浓)=S↓+SO2↑+2H2O中,化合价的变化为:H2S→S,S元素由-2价→0价,一个H2S分子失去2个电子,所以H2S是还原剂;S是氧化产物;H2SO4→SO2,S元素由+6价→+4价,一个H2SO4分子得2个电子,该反应中转移电子数为2,以此来解答;
(3)反应③中Mn元素化合价降低,Cl元素化合价升高;
(4)根据得失电子配平方程式,根据氧化剂和氯气之间的关系式判断,配平为2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O.
解答 解:(1)反应①中只有Cl元素化合价发生变化,Cl元素化合价由0价分别分别变化为+5价、-1价,被氧化与被还原的氯元素的质量之比为1:5,所以氧化剂与还原剂的质量之比为5:1,故答案为:5:1;
(2)②中,化合价的变化为:H2S→S,S元素由-2价→0价,一个H2S分子失去2个电子,所以H2S是还原剂;S是氧化产物;H2SO4→SO2,S元素由+6价→+4价,一个H2SO4分子得2个电子, ,故答案为:
,故答案为: ;
;
(3)反应③中Mn元素化合价降低,Cl元素化合价升高,由方程式可知当有4molHCl参加反应,有2mol被氧化,被氧化和未被氧化的Cl-的个数比为1:1,
故答案为:1:1;
(4)根据得失电子配平方程式,根据氧化剂和氯气之间的关系式判断,配平为2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O,故答案为:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O.
点评 本题综合考查氧化还原反应,为高频考点,侧重于学生的分析、计算能力的考查,注意把握氧化还原反应的相关概念与化合价的关系,难度不大.

练习册系列答案
相关题目
15.下列实验中能达到预期目的是( )
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
②用NaOH溶液除去苯中的少量苯酚
③高级脂肪酸钠溶液中混有丙三醇(盐析,过滤)
④用加热的方法提取NH4Cl固体中混有的少量碘
⑤用醋和澄清石灰水验证蛋壳中含有碳酸盐
⑥用米汤检验食用加碘盐中含碘
⑦用碘酒验证汽油中含有不饱和烃.
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
②用NaOH溶液除去苯中的少量苯酚
③高级脂肪酸钠溶液中混有丙三醇(盐析,过滤)
④用加热的方法提取NH4Cl固体中混有的少量碘
⑤用醋和澄清石灰水验证蛋壳中含有碳酸盐
⑥用米汤检验食用加碘盐中含碘
⑦用碘酒验证汽油中含有不饱和烃.
| A. | ①②③⑦ | B. | ①③⑤⑥⑦ | C. | ②③⑤⑦ | D. | ②③④⑤⑦ |
13.一种盐X与烧碱混合共热,可放出无色气体Y,Y经一系列氧化后的产物再溶于水可得Z溶液,Y和Z溶液反应又可生成X,则盐X是( )
| A. | NH4NO3 | B. | NH4Cl | C. | (NH4)2SO4 | D. | NH4HCO3 |
20.有机物M的结构简式为  ,下列有关M性质的叙述中错误的是( )
,下列有关M性质的叙述中错误的是( )
 ,下列有关M性质的叙述中错误的是( )
,下列有关M性质的叙述中错误的是( )| A. | M与金属钠完全反应时,二者物质的量之比为1:2 | |
| B. | M与碳酸氢钠完全反应时,二者物质的量之比为1:1 | |
| C. | M与氢氧化钠完全反应时,二者物质的量之比为1:2 | |
| D. | M既能与乙酸反应,又能与乙醇反应 |
10.下列物质中,能导电的有①⑤,属于电解质的③④⑦⑩,属于非电解质的是②⑥⑨
①Cu ②液氨 ③AgCl ④NaC1晶体 ⑤硫酸溶液 ⑥干冰 ⑦BaSO4⑧金刚石 ⑨蔗糖 ⑩冰醋酸(纯CH3COOH)
①Cu ②液氨 ③AgCl ④NaC1晶体 ⑤硫酸溶液 ⑥干冰 ⑦BaSO4⑧金刚石 ⑨蔗糖 ⑩冰醋酸(纯CH3COOH)
3.下列关于微粒半径的叙述中,正确的是( )
| A. | 金属阳离子的半径大于它的原子半径 | |
| B. | 金属阳离子的半径小于它的原子半径 | |
| C. | 非金属阴离子的半径小于其原子半径 | |
| D. | 核外电子排布相同的不同微粒,核电荷数越大半径越小 |
20.下列事实中,不能说明氯的非金属性比硫强的是( )
| A. | 高氯酸(HClO4)的酸性比硫酸强 | B. | 次氯酸的氧化性比稀硫酸强 | ||
| C. | 氯化氢比硫化氢的热稳定性好 | D. | 硫离子还原性比氯离子还原性强 |
1.下列关于离子键、共价键的叙述中正确的是( )
| A. | 在离子化合物里,只存在离子键,没有共价键 | |
| B. | 非极性键只存在于双原子的单质分子(如Cl2)中 | |
| C. | 由多种元素组成的多原子分子里,一定只存在极性键 | |
| D. | 在共价化合物分子内,一定不存在离子键 |
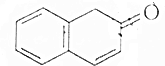
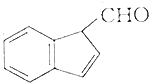
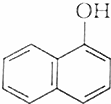
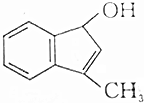
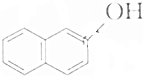 ,下列化合物中,不是2-奈酚的同分异构体的是( )
,下列化合物中,不是2-奈酚的同分异构体的是( )