题目内容
难溶化合物的溶解能力可以用溶度积Ksp来表示,当溶液中相应离子浓度的乘积大于该值时,会形成沉淀.已知常温下AgCl的Ksp=1.8×10-10,AgI的Ksp=8.5×10-17.若在常温下,向5mL含有KCl和KI各为0.01mol/L的溶液中加入8mL 0.01mol/L AgNO3溶液,此时溶液中所含溶质的离子浓度大小关系正确的是( )
| A、c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-) |
| B、c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| C、c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) |
| D、c(K+)>c(NO3-)>c(Ag+)=c(Cl-)+c(I-) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:KKsp(AgI)<Ksp(AgCl),所以先生成AgI,再生成AgCl,AgNO3+KI═AgI↓+KNO3,n(KI)=0.01mol?L-1×5 mL=5.0×10-5 mol,消耗n(AgNO3)=5.0×10-5mol,AgNO3+KCl═AgCl↓+KNO3,过量的AgNO3为0.01 mol?L-1×8 mL-5.0×10-5 mol=3.0×10-5 mol,而KCl为n(KCl)=0.01mol?L-1×5 mL=5.0×10-5 mol,则KCl过量,生成AgCl为3.0×10-5 mol,由此得出反应后溶液中的溶质为KNO3、KCl,生成AgCl、AgI沉淀.
解答:
解:A.Ksp(AgI)<Ksp(AgCl),所以先生成AgI,再生成AgCl,AgNO3+KI═AgI↓+KNO3,n(KI)=0.01mol?L-1×0.005 L=5.0×10-5 mol,消耗n(AgNO3)=5.0×10-5mol,AgNO3+KCl═AgCl↓+KNO3,过量的AgNO3为0.01 mol?L-1×0.008 L-5.0×10-5 mol=3.0×10-5 mol,而KCl为n(KCl)=0.01mol?L-1×0.005 L=5.0×10-5 mol,则KCl过量,生成AgCl为3.0×10-5 mol,由此得出反应后溶液中的溶质为KNO3、KCl,
n(KNO3)=n(AgNO3)=0.01 mol?L-1×0.008 L=8×10-5 mol,n(KCl)=5.0×10-5 mol,
根据物料守恒得离子浓度大小顺序是c(K+)>c(NO3-)>c(Cl-),溶液中还存在氯离子,所以银离子浓度较小,碘化银溶度积常数最小,所以碘离子浓度最小,所以离子浓度大小顺序是c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-),故A正确;
B.氯化钾还有剩余,所以c(Cl-)>c(Ag+),故B错误;
C.根据物料守恒得c(K+)>c(NO3-),故C错误;
D.溶液中还有氯离子剩余,所以c(Cl-)>c(Ag+),故D错误;
故选A.
n(KNO3)=n(AgNO3)=0.01 mol?L-1×0.008 L=8×10-5 mol,n(KCl)=5.0×10-5 mol,
根据物料守恒得离子浓度大小顺序是c(K+)>c(NO3-)>c(Cl-),溶液中还存在氯离子,所以银离子浓度较小,碘化银溶度积常数最小,所以碘离子浓度最小,所以离子浓度大小顺序是c(K+)>c(NO3-)>c(Cl-)>c(Ag+)>c(I-),故A正确;
B.氯化钾还有剩余,所以c(Cl-)>c(Ag+),故B错误;
C.根据物料守恒得c(K+)>c(NO3-),故C错误;
D.溶液中还有氯离子剩余,所以c(Cl-)>c(Ag+),故D错误;
故选A.
点评:本题以难溶物的溶解平衡为载体考查了离子浓度大小比较,明确物质之间发生的反应及反应后溶液中的溶质是解本题关键,再结合物料守恒判断离子浓度大小,题目难度较大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
BHT是一种常用的食品抗氧化剂,从 出发合成BHT的方法有如图两种.下列说法错误的是( )
出发合成BHT的方法有如图两种.下列说法错误的是( )

 出发合成BHT的方法有如图两种.下列说法错误的是( )
出发合成BHT的方法有如图两种.下列说法错误的是( )
| A、两种方法的反应类型都是加成反应 |
| B、BHT在水中的溶解度小于苯酚 |
C、BHT与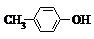 都能使酸性KMnO4褪色 都能使酸性KMnO4褪色 |
| D、从绿色化学角度分析方法一优于方法二 |
在试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是( )
| A、滴有酚酞的Na2CO3溶液 |
| B、溶有SO2的品红溶液 |
| C、滴有石蕊的AlCl3溶液 |
| D、滴有酚酞的饱和Ca(OH)2溶液 |
2008年北京奥运会“祥云”火炬用的是环保型燃料--丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷.下列有关说法不正确的是( )
| A、丙烷和丁烷互为同系物,化学性质相似 |
| B、丙烷和丁烷的特征反应均为取代反应 |
| C、C3H8没有同分异构体,C4H10有两种同分异构体 |
| D、等质量的丙烷和丁烷完全燃烧时,后者耗氧量大 |
 图为一种铜锌原电池的示意图,A中盛ZnSO4溶液并插入锌片,B中盛CuSO4溶液并插入铜片,“盐桥”是一支U型管,内装用饱和KCl溶液和琼脂混合制成的胶状溶液,其作用是形成闭合回路.该原电池工作时电流计指针偏转,溶液始终保持电中性,则下列说法正确的是( )
图为一种铜锌原电池的示意图,A中盛ZnSO4溶液并插入锌片,B中盛CuSO4溶液并插入铜片,“盐桥”是一支U型管,内装用饱和KCl溶液和琼脂混合制成的胶状溶液,其作用是形成闭合回路.该原电池工作时电流计指针偏转,溶液始终保持电中性,则下列说法正确的是( )| A、导线上的电流方向为A→B |
| B、A中SO42-浓度有所减小 |
| C、盐桥中Cl-向A中移动 |
| D、B中铜片质量有所增加 |
有 Fe3+、Fe2+、NO3-、NH4+、H+和H2O六种微粒,分别属于一个氧化还原反应中的反应物和生成物,下列叙述中,不正确的是( )
| A、还原产物为NH4+ |
| B、氧化剂与还原剂的物质的量之比为1:8 |
| C、若有0.5mol NO3-参加还原反应,则转移电子8mol |
| D、若把该反应设计为电解池,则阳极反应为Fe2+-e→Fe3+ |
下列条件下,离子能大量共存或者离子方程式正确的是( )
| A、pH=1的溶液中:Fe2+、ClO-、Na+、SO42- |
| B、在含较多Al3+的溶液中:K+、Cl-、HCO3- |
| C、一小块钠投入到CuSO4溶液中:2Na+Cu2+═Cu+2Na+ |
| D、铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
