题目内容
13.同温同压下,体积比为1:2:3所组成的N2、O2和CO2混合气体33.6g在标准状况下体积为20.16 L.分析 体积之比等于物质的量之比,结合总质量计算各物质相应物质的量,再根据V=nVm计算混合气体在标准状况下的体积.
解答 解:同温同压下,体积比为1:2:3所组成的N2、O2和CO2的物质的量之比为1:2:3,设氮气物质的量为n mol,则28n+2n×32+3n×44=33.6,解得:n=0.15,
故标况下混合气体总体积为:0.15mol×(1+2+3)×22.4L/mol=20.16L,
故答案为:20.16.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与气体摩尔体积之间的关系即可解答,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
相关题目
3.设NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 2.4g镁的原子核外电子数为0.2NA | |
| B. | 2.3 g Na与氧气反应生成Na2O和Na2O2,转移电子数为0.1NA | |
| C. | 1mol丙烷分子中11 mol共价键 | |
| D. | 1.4 g C2H4和C3H6的混合气体中,含0.2NA的C原子 |
4.1.42g R元素可与氧元素组成2.38g氧化物X,或组成3.66g氧化物Y,则X、Y的化学式可能是( )
| A. | R2O和R2O5 | B. | R2O3和R2O5 | C. | R2O3和R2O7 | D. | R2O和R2O3 |
1.有关有机物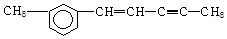 ,说法正确的是( )
,说法正确的是( )
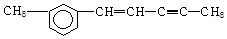 ,说法正确的是( )
,说法正确的是( )| A. | 该有机物属于脂肪烃 | |
| B. | 该有机物的分子式为:C12H14 | |
| C. | 该有机物可与5molH2发生加成反应 | |
| D. | 分子中,处于同一平面上的碳原子数最多可能有12个 |
8.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1 KSCN溶液中:Fe3+、NH4+、Br-、SO42- | |
| B. | $\frac{{c(O{H^-})}}{{c({H^+})}}$=106的溶液中:NH4+、K+、AlO2-、NO3- | |
| C. | 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl- | |
| D. | 0.1 mol•L-1 Ca(NO3)2溶液中:Na+、NH4+、CO32-、CH3COO- |
