题目内容
工业中常用氨水吸收尾气中的SO2,再向所得产物中加入稀硫酸回收SO2,有关反应的离子方程式为 .
考点:离子方程式的书写,二氧化硫的化学性质
专题:
分析:二氧化硫与氨水反应生成亚硫酸铵;亚硫酸铵与硫酸反应生成硫酸铵、二氧化硫和水,据此解答.
解答:
解:二氧化硫与氨水反应生成亚硫酸铵,离子方程式为:2NH3?H2O+SO2=2NH4++SO32-+H2O;
亚硫酸铵与硫酸反应生成硫酸铵、二氧化硫和水,离子方程式为:SO32-+2H+=SO2+H2O;
故答案为:2NH3?H2O+SO2=2NH4++SO32-+H2O;SO32-+2H+=SO2+H2O.
亚硫酸铵与硫酸反应生成硫酸铵、二氧化硫和水,离子方程式为:SO32-+2H+=SO2+H2O;
故答案为:2NH3?H2O+SO2=2NH4++SO32-+H2O;SO32-+2H+=SO2+H2O.
点评:本题考查了离子方程式的书写,明确发生的反应是解题关键,注意化学式的拆分、原子个数守恒.

练习册系列答案
相关题目
下列实验获得成功的是( )
| A、欲证明放入硫酸溶液中的纤维素加热已发生水解,可向所得溶液加入银氨溶液,放在水浴中 |
| B、欲证明淀粉的水解产物为葡萄糖,可向试管中加入0.5克淀粉及20%的稀硫酸4ml,加热3-4分钟,再向试管中加入新制Cu(OH)2 煮沸,观察有机红色沉淀生成 |
| C、为证明硬脂酸有酸性,取稀NaOH溶液加入硬脂酸并加热 |
| D、用灼烧的方法检验是毛线还是棉线 |
阿司匹林是一种常用的解热镇痛药,当它在碱性条件下完全水解时,可得到的全部产物有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
火箭使用的燃料是偏二甲肼(C2H8N2),火箭升空时发生的化学反应为:C2H8N2+2N2O4=2CO2↑+3N2↑+4H2O↑.下列有关该反应的说法正确的是( )
| A、该反应的氧化剂是偏二甲肼 |
| B、该反应进行时只有放热过程没有吸热过程 |
| C、该反应中氮元素的化合价升高 |
| D、该反应中每生成1mol CO2转移8mol电子 |

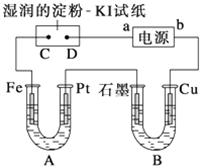 电解装置如图所示.图中B装置盛1L 2mol?L-1的Na2SO4溶液,A装置中盛1L 2mol?L-1AgNO3溶液.通电后,湿润的淀粉KI试纸的C端变蓝色.电解一段时间后,试回答:
电解装置如图所示.图中B装置盛1L 2mol?L-1的Na2SO4溶液,A装置中盛1L 2mol?L-1AgNO3溶液.通电后,湿润的淀粉KI试纸的C端变蓝色.电解一段时间后,试回答: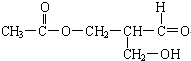 在有机物分子中碳原子所连的4个原子或原子团均不相同时,该碳原子叫手性碳原子,以*C表示.而且,该有机化合物具有光学活性.下列有机物是否具有光学活性?
在有机物分子中碳原子所连的4个原子或原子团均不相同时,该碳原子叫手性碳原子,以*C表示.而且,该有机化合物具有光学活性.下列有机物是否具有光学活性?