题目内容
2.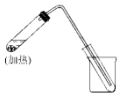 如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:(1)先取少量自来水于试管中,加入HNO3酸化的AgNO3,发现自来水变浑浊,说明自来水中含有Cl-.
(2)左边大试管中要加入几片碎瓷片,其作用是防止暴沸;
(3)该装置中使用的玻璃导管较长,其作用是冷凝气体;
(4)取少量制取出的蒸馏水于试管中,再次加入HNO3酸化的AgNO3,没有发现明显现象,说明蒸馏水中不再含有Cl-.
分析 (1)和硝酸银应反应生成白色不溶于硝酸的白色沉淀只有氯化银;
(2)水的沸点为100℃,制取少量蒸馏水,为防止液体暴沸,应加碎瓷片;
(3)玻璃导管除了起导气的作用,还起到了冷凝的作用;
(4)氯离子与银离子反应生成不溶于硝酸的氯化银白色沉淀,再次加入HNO3酸化的AgNO3,没有发现明显现象,说明蒸馏水中不再含有Cl-.
解答 解:(1)先取少量自来水于试管中,加入HNO3酸化的AgNO3,自来水变浑浊,说明有不溶于硝酸的沉淀生成,不溶于硝酸的白色沉淀只有氯化银,则一定是氯化银,证明自来水中含有氯离子,
故答案为:自来水中含有Cl-;
(2)左边大试管中要加入几片碎瓷片,碎瓷片具有疏松多孔结构,能作汽化中心,其作用是防止液体暴沸,
故答案为:防止暴沸;
(3)该装置中使用的玻璃导管较长,其作用除了起导气的作用外,还起冷凝水蒸气作用,
故答案为:冷凝气体;
(4)氯离子与银离子反应生成不溶于硝酸的氯化银白色沉淀,再次加入HNO3酸化的AgNO3,没有发现明显现象,说明蒸馏水中不再含有Cl-,
故答案为:蒸馏水中不再含有Cl-.
点评 本题考查实验室制备蒸馏水操作,题目难度不大,本题注意实验操作要点,学习中注意正确操作方法和实验的注意事项,注意氯离子的检验方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
10.阿司匹林是一种常用的解热镇痛药,其结构如图所示,根据其结构推断,其可能有的性质为( )
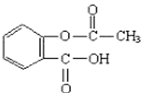

| A. | 该物质能与浓溴水发生取代反应 | B. | 该物质能发生酯化反应 | ||
| C. | 该物质属于蛋白质 | D. | 该物质极易溶于水和有机溶剂 |
17.同温同压下,相同体积的下列气体中,质量最大的是( )
| A. | 氯气 | B. | 氢气 | C. | 氧气 | D. | 氮气 |
7.分类是化学研究的重要方法,下列物质分类错误的是( )
| A. | 化合物:干冰,明矾,烧碱 | B. | 同素异形体:C60,石墨,金刚石 | ||
| C. | 非电解质:乙醇,四氯化碳,氯气 | D. | 混合物:纯净矿泉水,盐酸,漂白粉 |
14.过氧化钠可作为氧气的来源,常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
| 选项 | 二氧化碳 | 碳酸钠 | 转移的电子 |
| A | lmol | 2NA | |
| B | 22.4L | lmol | |
| C | 106g | lmol | |
| D | 106g | 2NA |
| A. | A | B. | B | C. | C | D. | D |
12.下列叙述正确的是( )
| A. | 不同元素的原子结构的分子只含极性共价键 | |
| B. | 137Cs和133Cs是中子数不同质子数相同的同种核素 | |
| C. | ⅠA族元素的金属性比ⅡA族元素的金属性强 | |
| D. | 同周期元素(除0族元素外)从左到右,原子半径逐渐减小 |