题目内容
某醇烯酸是合成香精的主要原料,其结构简式为: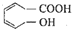 下列有关该醇烯酸的叙述正确的是( )
下列有关该醇烯酸的叙述正确的是( )
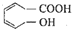 下列有关该醇烯酸的叙述正确的是( )
下列有关该醇烯酸的叙述正确的是( )| A、该醇烯酸的分子式为C7H8O3 |
| B、既可以通过加聚反应形成高分子,也可以通过缩聚反应形成高分子 |
| C、不能使酸性高锰酸钾溶液褪色 |
| D、分子内能形成六元环的酯 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:有机物含有羟基、可发生取代、氧化和消去反应,含有羧基,具有酸性,可发生中和、酯化反应,含有碳碳双键,可发生加成、加聚和氧化反应,有机物含有羟基和羧基,可发生缩聚反应,以此解答.
解答:
解:A.由结构简式可知有机物分子式为C7H10O3,故A错误;
B.分子中含有碳碳双键,可发生加聚反应,含有羟基和羧基,可发生缩聚反应,故B正确;
C.分子中含有碳碳双键,可与酸性高锰酸钾溶液发生氧化还原反应,故C错误;
D.分子中含有羧基和羟基,可发生酯化反应,可形成七元环的酯,故D错误.
故选B.
B.分子中含有碳碳双键,可发生加聚反应,含有羟基和羧基,可发生缩聚反应,故B正确;
C.分子中含有碳碳双键,可与酸性高锰酸钾溶液发生氧化还原反应,故C错误;
D.分子中含有羧基和羟基,可发生酯化反应,可形成七元环的酯,故D错误.
故选B.
点评:本题考查有机物的结构与性质,为高考高频考点,把握结构中官能团与性质的关系为解答的关键,注意信息的利用及分析,侧重羧酸性质的考查,题目难度不大.

练习册系列答案
相关题目
 生物质(通过光合作用产生的有机体)是一种可再生能源,能发生如图转化.下列说法不正确的是( )
生物质(通过光合作用产生的有机体)是一种可再生能源,能发生如图转化.下列说法不正确的是( )| A、沼气的主要成分是甲烷 |
| B、汽油属于一次能源 |
| C、乙醇属于可再生能源 |
| D、生物质能来源于太阳能 |
下列除去杂质的方法正确的是( )
| A、除去氨气中的水蒸气:气体通过装有浓硫酸的洗气瓶 |
| B、除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶 |
| C、除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤 |
| D、除去Cu粉中混有的CuO:加适量稀硝酸后,过滤.洗涤 |
已知一定条件下,CO2 和CO的混合气体对氢气的相对密度是20,则CO2 和CO的质量比为( )
| A、1:3 | B、33:7 |
| C、3:1 | D、7:33 |
下列说法正确的是( )
| A、室温时某溶液的pH<7,则该物质一定是酸或强酸弱碱盐 |
| B、已知室温时,0.1mol?L-1某一元酸HA的电离平衡常数为1×10-7,则该酸的电离度约为0.01% |
| C、0.02mol?L-1CH3COOH溶液和0.01mol?L-1NaOH溶液等体积混合,则溶液中:2c(H+)+c(CH3COOH)=2c(OH-)+c(CH3COO-) |
| D、在温度不变的条件下向CaSO4饱和溶液中加入Na2SO4溶液,CaSO4将会析出,但Ksp不会发生改变 |
自瑞士ETH天文研究所的Ansgar Grimberg等的研究结果表明,太阳气体中存在大量的20Ne和22Ne.下列关于20Ne和22Ne的说法正确的是( )
| A、20Ne和22Ne互为同位素 |
| B、20Ne和22Ne是同一种核素 |
| C、20Ne的原子核中有20个质子 |
| D、22Ne的原子核中有22个中子 |
化学与环境、材料、能源关系密切,下列说法正确的是( )
| A、装饰材料释放的苯、甲苯、甲醛等易挥发性烃类物质会导致室内空气污染 |
| B、塑化剂是一种应用很广的化工塑料软化剂,可大量添加到婴幼儿玩具中 |
| C、PM 2.5亦称可入肺颗粒物,表面积大,能吸附有毒有害物质 |
| D、汽油标准已由“国Ⅲ”提到“国Ⅳ”,这意味着汽车不再排放氮氧化物 |
 电子产品小型化、微型化、集成化是当今世界技术发展的大势所趋,对锂离子二次电池提出了更高比容量的要求,锂硫电池的理论能量密度为是锂离子二次电池的3-5倍,是极具应用前景的电化学储能体系,近年来引起了研究人员的广泛关注.锂硫电池常用有机溶剂碳酸酯类(
电子产品小型化、微型化、集成化是当今世界技术发展的大势所趋,对锂离子二次电池提出了更高比容量的要求,锂硫电池的理论能量密度为是锂离子二次电池的3-5倍,是极具应用前景的电化学储能体系,近年来引起了研究人员的广泛关注.锂硫电池常用有机溶剂碳酸酯类(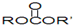 )作为电解质溶液,放电时某极的电极反应式为:S+2Li+2e-═Li2S,电池如图所示:图中①②曲线为Li+移动方向.以下说法不正确的是( )
)作为电解质溶液,放电时某极的电极反应式为:S+2Li+2e-═Li2S,电池如图所示:图中①②曲线为Li+移动方向.以下说法不正确的是( )| A、放电时Li+移动方向与曲线①一致 |
| B、电解质溶液不能用醋酸溶液代替碳酸酯类 |
| C、充电时阴极反应式:Li++e-═Li |
| D、充电时b电极接电源的正极 |
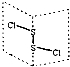 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )| A、S2Cl2的结构中各原子均达到8电子的稳定结构 |
| B、S2Cl2为含有极性键和非极性键的共价化合物 |
| C、若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2>S2Br2 |
| D、S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl |