题目内容
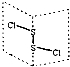 二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2遇水易与水发生反应,并产生能使品红褪色的气体.下列说法错误的是( )| A、S2Cl2的结构中各原子均达到8电子的稳定结构 |
| B、S2Cl2为含有极性键和非极性键的共价化合物 |
| C、若S2Br2与S2Cl2结构相似,则熔沸点:S2Cl2>S2Br2 |
| D、S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
考点:不同晶体的结构微粒及微粒间作用力的区别,极性键和非极性键
专题:化学键与晶体结构
分析:A、由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,写出电子式确定每个原子周围的电子数;
B、同种元素原子之间形成非极性键,不同元素的原子之间形成的化学键为极性键;
C、组成与结构相似,相对分子质量越大,分子间作用力越强;
D、S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理.
B、同种元素原子之间形成非极性键,不同元素的原子之间形成的化学键为极性键;
C、组成与结构相似,相对分子质量越大,分子间作用力越强;
D、S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理.
解答:
解:A.由A、由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S2Cl2的电子式为  ,每个原子周围都满足8电子稳定结构,故A正确;
,每个原子周围都满足8电子稳定结构,故A正确;
B.S2Cl2分子中S-S为非极性键,S-Cl键为极性键,所以S2Cl2为含有极性键和非极性键的共价化合物,故B正确;
C.组成与结构相似,相对分子质量越大,分子间作用力越强,所以S2Cl2<S2Br2,故C错误;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理,则S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl,故D正确.
故选C.
 ,每个原子周围都满足8电子稳定结构,故A正确;
,每个原子周围都满足8电子稳定结构,故A正确;B.S2Cl2分子中S-S为非极性键,S-Cl键为极性键,所以S2Cl2为含有极性键和非极性键的共价化合物,故B正确;
C.组成与结构相似,相对分子质量越大,分子间作用力越强,所以S2Cl2<S2Br2,故C错误;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),符合氧化还原反应原理,则S2Cl2与H2O反应的化学方程式可能为:2S2Cl2+2H2O═SO2↑+3S↓+4HCl,故D正确.
故选C.
点评:本题以S2Cl2的结构为载体,考查分子结构、化学键、电子式、氧化还原反应等,难度不大,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
某醇烯酸是合成香精的主要原料,其结构简式为: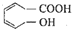 下列有关该醇烯酸的叙述正确的是( )
下列有关该醇烯酸的叙述正确的是( )
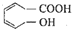 下列有关该醇烯酸的叙述正确的是( )
下列有关该醇烯酸的叙述正确的是( )| A、该醇烯酸的分子式为C7H8O3 |
| B、既可以通过加聚反应形成高分子,也可以通过缩聚反应形成高分子 |
| C、不能使酸性高锰酸钾溶液褪色 |
| D、分子内能形成六元环的酯 |
下列有关物质性质的应用正确的是( )
| A、液氨汽化时要放出大量的热,可用作制冷剂 |
| B、二氧化硫可广泛用于食品的漂白 |
| C、生石灰能与水反应,可用来干燥氯气 |
| D、氧化铝是一种电解质,可用于制铝 |
下列因果关系叙述正确的是( )
| A、SO2具有漂白性,故可使酸性KMnO4溶液褪色 |
| B、浓硝酸中的HNO3见光会分解,故有时在实验室看到的浓硝酸呈黄色 |
| C、Na的金属性比Cu强,故可用Na与CuSO4溶液反应制取Cu |
| D、Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中Fe也显+3价 |
如图为一原电池的结构示意图,下列说法不正确的是( )
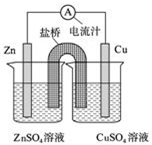

| A、原电池工作时的总反应为Zn+Cu2+═Zn2++Cu |
| B、原电池工作时,Zn电极流出电子,发生氧化反应 |
| C、若将Cu电极改为Fe电极,CuSO4溶液改为FeSO4溶液,Zn电极仍作负极 |
| D、盐桥中装有琼脂-饱和氯化钾溶液,则盐桥中的K+移向ZnSO4溶液 |
 硼化钒一空气电池是目前储电能力最高的电池,其示意图如图所示,该电池工作时的反应为4VB2+11O2═4B2O3+2V2O5.下列说法正确的是( )
硼化钒一空气电池是目前储电能力最高的电池,其示意图如图所示,该电池工作时的反应为4VB2+11O2═4B2O3+2V2O5.下列说法正确的是( )| A、电极X为电池负极 |
| B、OH-向电极X移动 |
| C、1mol VB2反应转移的电子数目是锂电池1mol Li反应转移的11倍 |
| D、VB2极的电极反应为2VB2+22e-+11H2O═2B2O3+V2O5+22OH- |
对于常温下pH=12的氨水,下列说法正确的是( )
| A、由水电离产生的c(OH-)=10-12mol?L-1 | ||
| B、向溶液中加入适量盐酸使混合液的pH=7,混合液中c(NH4+)>c(Cl-) | ||
| C、等体积pH=12的氨水和pH=12的NaOH溶液可中和等物质的量的HCl | ||
D、用水稀释时,溶液中
|
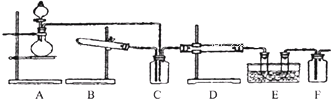
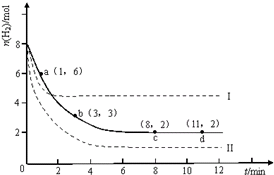 固定和利用CO2能有效地利用资源,并减少空气中的温室气体.工业上有一种用CO2来生产甲醇燃料的发法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1.某科学实验将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图所示(实线).
固定和利用CO2能有效地利用资源,并减少空气中的温室气体.工业上有一种用CO2来生产甲醇燃料的发法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ?mol-1.某科学实验将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图所示(实线).