题目内容
臭氧的化学式为O3.a molO3和a molO2具有相同的( )
| A、原子数 | B、分子数 |
| C、体积 | D、质量 |
考点:物质的量的相关计算
专题:计算题
分析:A.根据化学式计算原子物质的量进行判断;
B.根据N=nNA可知,物质的量相等,含有分子数目相等;
C.物质的量一定,温度、压强会影响气体的体积;
D.根据m=nM进行判断.
B.根据N=nNA可知,物质的量相等,含有分子数目相等;
C.物质的量一定,温度、压强会影响气体的体积;
D.根据m=nM进行判断.
解答:
解:A.a molO3含有3a mol氧原子,a molO2含有2a mol氧原子,而含有氧原子数目不相等,故A错误;
B.根据N=nNA可知,a molO3和a molO2含有分子数目相等,故B正确;
C.物质的量一定,温度、压强会影响气体的体积,二者所处条件下的气体摩尔体积不一定相等,二者占有的体积不一定相等,故C错误;
D.臭氧、氧气的摩尔质量不相等,根据m=nM可知,a molO3和a molO2的质量之比为3:2,二者质量不相等,故D错误,
故选B.
B.根据N=nNA可知,a molO3和a molO2含有分子数目相等,故B正确;
C.物质的量一定,温度、压强会影响气体的体积,二者所处条件下的气体摩尔体积不一定相等,二者占有的体积不一定相等,故C错误;
D.臭氧、氧气的摩尔质量不相等,根据m=nM可知,a molO3和a molO2的质量之比为3:2,二者质量不相等,故D错误,
故选B.
点评:本题考查物质的量有关计算,比较基础,注意理解温度、压强对气体摩尔体积的影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在光照条件下,将a mol甲烷与足量Cl2反应,测知四种产物的物质的量比依次2:1:1:2,则耗Cl2的物质的量为( )
| A、a mol |
| B、1.25a mol |
| C、2.5a mol |
| D、4a mol |
某无色溶液中可能含有I-、K+、Cu2+、SO32-(还原性:SO32->I-),向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是( )
①肯定不含I-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有I-.
①肯定不含I-; ②肯定不含Cu2+; ③肯定含有SO32-; ④可能含有I-.
| A、①③ | B、①②③ |
| C、②③④ | D、①② |
微粒有多种表示方式,下列各组不同表示方式一定代表同种微粒的是( )
| A、C3H6、CH2=CHCH3 |
B、-OH、 |
C、 、 、 |
D、 、1s22s22p63s23p6 、1s22s22p63s23p6 |
用NA表示阿伏伽德罗常数的值,下列说法不正确的是( )
| A、常温下,1mol甲烷含有的氢原子数为4NA |
| B、2g氦气所含有原子数为0.5NA |
| C、0.1mol/L的硫酸铝溶液中含SO42-数为0.3NA |
| D、18g水所含质子数为10NA |
下列方程式书写正确的是( )
| A、醋酸的电离:CH3COOH+H2O?CH3COO-+H3O+ |
| B、H2SO3的电离方程式H2SO3?2H++SO32- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、CaCO3的电离方程式:CaCO3?Ca2++CO32- |
常温下,pH相同的NaOH溶液和CH3COONa溶液分别加水稀释.pH随溶液体积变化的曲线如图所示,则下列叙述正确的是( )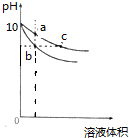

| A、b、c两点溶液的导电能力相同 |
| B、c点溶液中c (CH3COOH)+c(OH-)=c(H+) |
| C、a、b、c三点溶液中水的电离程度a>c>b |
| D、等体积的b、c两点溶液分别与相同浓度的盐酸恰好完全反应时,消耗盐酸的体积相等 |
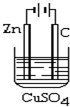 电解原理在工业有广泛的应用.利用相关知识回答下面的问题.
电解原理在工业有广泛的应用.利用相关知识回答下面的问题.