题目内容
下列除去杂质的方法中错误的是( )
| 物质 | 杂质 | 除杂质的方法 | |
| A | CaCl2溶液 | HCl | 过量CaCO3、过滤 |
| B | NaOH溶液 | Ca(OH)2 | 过量Na2CO3溶液、过滤 |
| C | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D | CO2 | H2O | 通过盛浓硫酸的洗气瓶 |
| A、A | B、B | C、C | D、D |
考点:物质的分离、提纯的基本方法选择与应用
专题:实验评价题
分析:A.CaCO3与盐酸反应生成氯化钙;
B.Na2CO3与氢氧化钙反应生成碳酸钙和NaOH,但Na2CO3过量;
C.Fe与CuCl2反应生成Cu、FeCl2;
D.浓硫酸具有吸水性,且不与二氧化碳反应.
B.Na2CO3与氢氧化钙反应生成碳酸钙和NaOH,但Na2CO3过量;
C.Fe与CuCl2反应生成Cu、FeCl2;
D.浓硫酸具有吸水性,且不与二氧化碳反应.
解答:
解:A.CaCO3与盐酸反应生成氯化钙,然后过滤可除杂,故A正确;
B.Na2CO3与氢氧化钙反应生成碳酸钙和NaOH,但Na2CO3过量,引入新的杂质碳酸钠,故B错误;
C.Fe与CuCl2反应生成Cu、FeCl2,然后过滤可除杂,故C正确;
D.浓硫酸具有吸水性,且不与二氧化碳反应,则通过盛浓硫酸的洗气瓶可除杂,故D正确;
故选B.
B.Na2CO3与氢氧化钙反应生成碳酸钙和NaOH,但Na2CO3过量,引入新的杂质碳酸钠,故B错误;
C.Fe与CuCl2反应生成Cu、FeCl2,然后过滤可除杂,故C正确;
D.浓硫酸具有吸水性,且不与二氧化碳反应,则通过盛浓硫酸的洗气瓶可除杂,故D正确;
故选B.
点评:本题考查物质分离、提纯方法的选择和应用,为高频考点,把握物质的性质及发生的反应、混合物分离提纯方法为解答的关键,侧重除杂的考查,题目难度不大.

练习册系列答案
相关题目
温室效应会导致全球变暖,其主要原因是( )
| A、CO2增多使太阳辐射到地球表面的能量增多 |
| B、植物的光合作用吸收了CO2 |
| C、CO2能放出能量,使地球变暖 |
| D、CO2、CH4等温室气体会吸收地球表面发出的长波辐射,减少地球的热量散失 |
阿伏加德罗常数约为6.02×1023mol-1,下列说法正确的是( )
| A、2.3g钠与足量丙三醇反应,转移电子数为0.3×6.02×1023 |
| B、标准状况下,22.4L乙醇的共价键数为8×6.02×1023 |
| C、标准状况下,5.6L甲醛所含的电子数为4×6.02×1023 |
| D、100mL 1mol?L-1醋酸溶液中,H+的个数为0.1×6.02×1023 |
下列事实不能用勒夏特列原理解释的是( )
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO,当加入NaOH溶液后,溶液颜色变浅 |
| B、对2HI(g)?H2(g)+I2(g)平衡体系,增大压强可使颜色变深 |
| C、汽水瓶盖打开后产生大量气泡 |
| D、工业合成氨工艺中,采用较高的压强来提高原料的转化率 |
银锌电池的电极分别是Ag2O和Zn,电解质溶液为KOH,它的放电过程表示为Ag2O+Zn+H2O═2Ag+Zn(OH)2下列叙述,正确的是( )
| A、在放电过程中,Ag2O为负极 |
| B、在放电过程中,电池负极区溶液pH减小 |
| C、在放电过程中,电子由Ag2O经外电路流向Zn |
| D、放电时,Ag2O电极发生氧化反应,Zn极发生还原反应 |
在H2与Cl2生成HCl的反应中,已知断裂1mol氢氢键吸收的能量为akJ,断裂1mol氯氯键吸收的能量为bkJ,形成1mol氢氯键放出的能量为ckJ,则生成1molHCl放出的能量为( )
| A、(c-a-b)kJ |
| B、(a+b-c)kJ |
| C、(2c-a-b)kJ |
| D、(2c-a-b)/2kJ |
共价键、离子键和分子间作用力是微粒之间的三种作用力.下列晶体①Ba(OH)2②SiO2③金刚石④KCl ⑤干冰中,含有两种作用力的是( )
| A、①②③ | B、①⑤ |
| C、②④⑤ | D、②③④ |
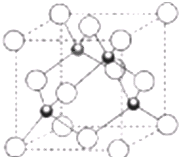 原子序数小于36的X、Y、Z、W四种元素,其中X是周期表中半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.
原子序数小于36的X、Y、Z、W四种元素,其中X是周期表中半径最小的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.