题目内容
8.下列说法中,正确的是( )| A. | 在任何条件下,纯水的pH=7 | |
| B. | 盐类对水的电离都有促进作用 | |
| C. | 在95℃时,纯水的pH>7 | |
| D. | 在95℃时,纯水中H+的物质的量浓度c(H+)>10-7mol/L |
分析 水的电离为吸热过程,加热促进数的电离,溶液中c(H+)增大,但仍满足c(H+)=c(OH-),以此解答该题.
解答 解:A.如温度高于常温,水的电离程度增大,则纯水的pH减小,可小于7,故A错误;
B.如盐不水解,则不促进水的电离,如为硫酸氢钠等盐,电离出氢离子,则抑制水的电离,故B错误;
C.升高温度,促进水的电离,在95℃时,纯水的pH<7,故C错误;
D.在95℃时,水的电离程度大于常温下,纯水中H+的物质的量浓度c(H+)>10-7mol/L,故D正确.
故选D.
点评 本题考查水的电离,为高频考点,侧重于学生的分析能力的考查,注意把握弱电解质的电离特点和影响因素,难度不大.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
4.下列含有非极性键的极性分子是( )
| A. | C2H5OH | B. | C2H2 | C. | HCOOH | D. | CH3OH |
19.实验室中需要配制2mol/L的NaCl溶液920mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
| A. | 920 mL,107.64 g | B. | 500 mL,117 g | ||
| C. | 1000 mL,117.0g | D. | 任意规格,107.64 g |
16.在80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4?2NO2△H>0,隔一段时间对该容器内的物质进行分析,得到如表数据:
(1)计算0~40s内用N2O4表示的平均反应速率为0.0025mol•L-1•s-1.
(2)计算在80℃时该反应的平衡常数K=1.8mol/L.
(3)40s时,NO2的浓度b=0.2mol/L,反应最迟到80s到达平衡状态
(4)反应进行至100s后将反应混合物的温度降低,混合气体的颜色变浅(填“变浅”“变深”或“不变”).
(5)要增大该反应的K值,可采取的措施有D(填序号).
A、增大N2O4的起始浓度B、向混合气体中通入NO2C、使用高效催化剂 D、升高温度.
| 时间/s n/mol | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)计算在80℃时该反应的平衡常数K=1.8mol/L.
(3)40s时,NO2的浓度b=0.2mol/L,反应最迟到80s到达平衡状态
(4)反应进行至100s后将反应混合物的温度降低,混合气体的颜色变浅(填“变浅”“变深”或“不变”).
(5)要增大该反应的K值,可采取的措施有D(填序号).
A、增大N2O4的起始浓度B、向混合气体中通入NO2C、使用高效催化剂 D、升高温度.
3.当光束通过下列分散系:①有尘埃的空气 ②稀硫酸 ③蒸馏水 ④墨水,能观察丁达尔效应的是( )
| A. | ①④ | B. | ②③ | C. | ①② | D. | ②④ |
20.表示下列粒子结构的图式,不正确的是( )
| A. | 乙烯的结构式: | B. | 钠离子的结构示意图: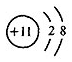 | ||
| C. | 氢分子的电子式:H:H | D. | 氯化氢分子的电子式: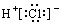 |
 $→_{①}^{Cl_{2},光照}$
$→_{①}^{Cl_{2},光照}$ $→_{②}^{NaOH,乙醇,△}$A$→_{③}^{溴水}$B$\stackrel{④}{→}$
$→_{②}^{NaOH,乙醇,△}$A$→_{③}^{溴水}$B$\stackrel{④}{→}$ $→_{⑤}^{Br_{2},催化剂}$
$→_{⑤}^{Br_{2},催化剂}$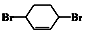 $\stackrel{⑥}{→}$
$\stackrel{⑥}{→}$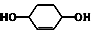
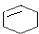 ,B的结构简式是
,B的结构简式是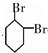 .
. .
.