题目内容
用H2O2和H2SO4的混合溶液可溶出废旧印刷电路板上的铜.已知:Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H1=+64.39kJ/mol2H2O2(l)═2H2O(l)+O2(g)△H2=-196.46kJ/molH2(g)+
O2(g)═H2O(l)△H3=-285.84kJ/mol求在H2SO4溶液中,Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热为多少?
| 1 |
| 2 |
考点:有关反应热的计算
专题:化学反应中的能量变化
分析:根据已知的热化学反应方程式和盖斯定律来分析Cu与H2O2反应生成Cu2+和H2O的热化学方程式,由盖斯定律①+
×②+③得到:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H,由盖斯定律可知该反应的反应热△H=H1+H2×
+H3,据此分析解答.
| 1 |
| 2 |
| 1 |
| 2 |
解答:
解:①Cu(s)+2H+(aq)═Cu2+(aq)+H2(g)△H=+64.39kJ/mol,
②2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ/mol,
③H2(g)+
O2(g)═H2O(l)△H=-285.84kJ/mol,
由盖斯定律①+
×②+③得到:Cu(s)+H2O2(l)+2H+(aq)═Cu2+(aq)+2H2O(l)△H=+64.39kJ/mol+
×(-196.46kJ/mol)+(-285.84kJ/mol)=-319.68kJ/mol,
答:Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热为:-319.68kJ/mol;
②2H2O2(l)═2H2O(l)+O2(g)△H=-196.46kJ/mol,
③H2(g)+
| 1 |
| 2 |
由盖斯定律①+
| 1 |
| 2 |
| 1 |
| 2 |
答:Cu与H2O2反应生成Cu2+(aq)和H2O(l)的反应热为:-319.68kJ/mol;
点评:本题考查反应热的有关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,明确反应热和化学计量数的关系是解题关键,题目难度不大.注意盖斯定律的应用.

练习册系列答案
相关题目
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度有关.下列各组物质:①Cu与HNO3溶液 ②Cu与FeCl3溶液 ③Zn与H2SO4溶液 ④Fe与HCl溶液.由于浓度不同而能发生不同氧化还原反应的是( )
| A、①③ | B、③④ | C、① | D、①③④ |
A2、B2、C23种单质和它们离子间能发生下列反应:①2A-+C2═2C-+A2 ②2C-+B2═2B-+C2,则有关说法中不正确的是( )
| A、氧化性:B2>C2>A2 |
| B、在含有C-和A-的溶液中加入B2,C-优先发生反应 |
| C、还原性:B->C->A- |
| D、在含有B2和C2的溶液中加入A-,B2优先发生反应 |
下列关于0.2mol/L硝酸钾溶液的叙述中,正确的是( )
| A、1L该溶液中含硝酸钾202g |
| B、100mL该溶液中含硝酸钾0.02mol |
| C、从1L该溶液中取出500mL后,剩余溶液的浓度为0.1mol/L |
| D、1L水中溶解0.2mol硝酸钾,即可配得0.2mol/L硝酸钾溶液 |
能正确表示下列反应的离子方程式是( )
| A、硫酸铝与过量氨水反应:Al3++4NH3?H2O═AlO2-+4NH4+ |
| B、将磁性氧化铁溶于盐酸:Fe3O4+8H+═2Fe3++Fe2++4H2O |
| C、将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-═Fe3++2H2O+NO↑ |
| D、硅酸钠溶液中通入过量CO2气体:SiO32-+H2O+CO2═H2SiO3↓+CO32- |
下列表述正确的是( )
A、H2O2的电子式: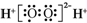 | ||
B、Cl的原子结构示意图: | ||
C、质子数是82,中子数是122的铅原子:
| ||
D、CO2的比例模型: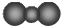 |
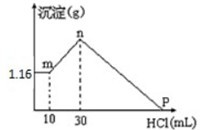 把由NaOH、AlCl3 和 MgCl2 三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向所得溶液里逐滴加入1mol?L-1的盐酸,加入盐酸的体积和沉淀的质量如图所示:
把由NaOH、AlCl3 和 MgCl2 三种固体组成的混合物溶于足量水中,有1.16g白色沉淀析出,向所得溶液里逐滴加入1mol?L-1的盐酸,加入盐酸的体积和沉淀的质量如图所示: