��Ŀ����
1��Ϊ̽��ͭ��Ũ����ķ�Ӧ���ס�����ͬѧ�ֱ������ͼ1��ͼ2��ʾװ�ã�������ͭ��10mL 18mol•L-1Ũ���Ṳ�ȣ�ֱ������������Ϊֹ���ٶ���Ӧǰ���Թ�����Һ��������䣩��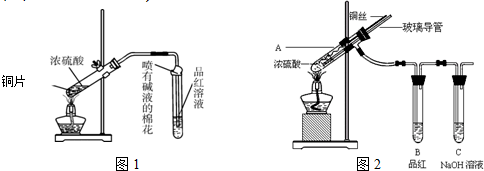
��1���Ƚ���ʵ��װ�ã�ͼ2װ�õ��ŵ��ǣ���ͨ��ͭ˿�����³鶯���Կ��Ʒ�Ӧ�ķ�����ֹͣ����ֹͣ����ʱ���ܷ�ֹ������ƽ��ѹǿ��
��2���ټ�����ѧ�Ļ�ѧ֪ʶ��Ϊ����һ����������ʣ�࣮����Ϊ����ʣ������������Ƿ�Ӧ��Ũ���ᱻ���ģ�ͬʱ����ˮ��Ũ������ϡ����Cu������ϡ���ᷴӦ��
������ҩƷ���ܹ�����֤����Ӧ���������ƿ��ȷ������ʣ�����AD����ѡ���ţ�
a���������� b���Ȼ�����Һ c������d��̼��������Һ
��3�����ڲ��ͼ2װ��ǰ����������Ϊʹװ���еIJ���������ȫ�����գ�Ӧ����ȡ�IJ����Ǵӵ��ܿ���A�д���������
��4��Ϊ�����ⶨ��ʣ������Ũ�Ȳ����ں�ֵʱ��ͭ������Ͳ��ܷ�Ӧ���ס�����λͬѧ������������ƣ�
�ټ����������������建��ͨ��Ԥ�ȳ�������ʢ�еļ�ʯ�Ҹ���ܣ���Ӧ�������ٴγ������������������ m g��ʣ����Ũ��Ϊ��18-$\frac{25m}{8}$��mol•L-1��
���ҷ������������Ӧ�����Һ��������ˮϡ����1 000mL��ȡ20.00mL����ƿ�У�����2��3�μ��ȣ���ѡ���̪���������ȡ�����0.1000mol•L-1��NaOH��Һ���еζ�����֪������ͭ��ʼ������pHԼΪ5������ȥNaOH��ҺV mL��������Ũ��Ϊ0.25Vmol•L-1��
�ۼס����������Ƚϣ�����Ϊ���ϴ���Ǽף������DZ���ʯ�����յij���SO2���ˮ����������SO2������ƫ�����������Ũ��ƫС��
���� ��1����ͼ1��ȣ�ͼ2 װ���У����Թ�ͭ˿�����³鶯���Կ��Ʒ�Ӧ�ķ�����ֹͣ��ֹͣ����ʱ���ܷ�ֹ������
��2�������ŷ�Ӧ�Ľ��У�Ũ�������ϡ���ᣬ��ϡ�����ͭ��Ӧ��
�����ᡢ����ͭ���ȱ��η�Ӧ�õ����ᱵ������Ag���������ᷴӦ��ʣ�����������Fe��̼�����Ʒ�Ӧ�������壬�ݴ˼����Ƿ�������ʣ�ࣻ
��3���ӵ��ܿ���A�д���������ʹ������������Һ�б�����Ϊ���
��4����ԭ����ͨ��������������أ��ⶨ���ɶ�������������������ø�������գ�����n=$\frac{m}{M}$���������������ʵ������ٸ��ݷ���ʽ����μӷ�Ӧ�������ʵ�������������ʣ������Ũ�ȣ�
���ҷ���������������ͭ��ʼ������pHԼΪ5�����ȵı�ɫ��ΧΪ3.1��4.4����̪�ı�ɫ��Χ��8.2��10������Ϊ�˼���ʵ����������к͵ζ�ʱѡ���ָʾ��Ϊ���ȣ���ʱֻ��������кͷ�Ӧ������n=cV����n��NaOH������������ʣ���������ʵ���Ũ�ȣ���������1000mL��Һ��ʣ���������ʵ������ٸ���c=$\frac{n}{V}$���㣻
�ۼס����������Ƚϣ���Ӧ����ʱ������SO2�����к���ˮ���������б���ʯ�����յij���SO2���ˮ����������SO2������ƫ��
��� �⣺��1���Ƚ���ʵ��װ�ã�ͼ2װ�õ��ŵ��ǣ���ͨ��ͭ˿�����³鶯����ʹ��Ӧ��ʱ������Ҳ�����Ƿ�Ӧ��ʱֹͣ�������Ϳ��Կ��ƻ�ѧ��Ӧ�Ľ��У���������ͼ2װ������һ���������ܣ���ֹͣ����ʱ������ƽ��ѹǿ�������Ϳ��Է�ֹ��������ķ�����
�ʴ�Ϊ��ͨ��ͭ˿�����³鶯���Կ��Ʒ�Ӧ�ķ�����ֹͣ��ֹͣ����ʱ���ܷ�ֹ������ƽ��ѹǿ����2���ٷ�Ӧ��Ũ���ᱻ���ģ�ͬʱ����ˮ��Ũ������ϡ����Cu������ϡ���ᷴӦ������һ����������ʣ�࣬
�ʴ�Ϊ����Ӧ��Ũ���ᱻ���ģ�ͬʱ����ˮ��Ũ������ϡ����Cu������ϡ���ᷴӦ��
��A����������ʣ�࣬�����Fe��ʱ�ᷢ����Ӧ��Fe+H2SO4=FeSO4+H2����ð���ݣ���A��ȷ��
B�������Ƿ�������ʣ�࣬����Һ�ж�����SO42-�������Ȼ�����Һʱ������Ӧ��Ba2++SO42-=BaSO4����������ɫ��������B����
C���ڽ������˳�����Ag��H�ĺ��棬���ܰ����е�H�û���������C����
D������H2SO4��H2CO3�����Լ���̼��������Һʱ������Ӧ��H2SO4+2NaHCO3=Na2SO4+2H2O+2CO2����ð����˵��������ʣ�࣬��D��ȷ��
��ѡ��AD��
��3�����ڲ��ͼ2װ��ǰ����������Ϊʹװ���еIJ���������ȫ�����գ�Ӧ����ȡ�IJ����Ǵӵ��ܿ���A�д���������ʹ������������Һ�б�����Ϊ���ᣬ
�ʴ�Ϊ���ӵ��ܿ���A�д���������
��4��������SO2���������壬��������Ӧ���ڼ����������������建��ͨ��Ԥ�ȳ�������ʢ�м�ʯ�ҵĸ���ܣ���Ӧ�������ٴγ������������������m g����n��SO2��=$\frac{m}{64}$mol����Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O����֪��Ӧ���ĵ���������ʵ���Ϊ$\frac{m}{64}$mol��2=$\frac{m}{32}$mol��ʣ����������ʵ���Ũ��Ϊ18mol/L-$\frac{\frac{m}{32}mol}{0.01L}$=��18-$\frac{25m}{8}$��mol/L��
�ʴ�Ϊ����ʯ�ң���18-$\frac{25m}{8}$��mol/L��
���ҷ���������������ͭ��ʼ������pHԼΪ5���ȵı�ɫ��ΧΪ3.1��4.4����̪�ı�ɫ��Χ��8.2��10������Ϊ�˼���ʵ����������к͵ζ�ʱѡ���ָʾ��Ϊ���ȣ���ʱֻ��������кͷ�Ӧ��n��NaOH��=V��10-3 L��0.1mol/L=V��10-4mol����ʣ����������ʵ���Ϊn��H2SO4��=$\frac{1}{2}$n��NaOH��=5V��10-5mol������������Ũ��Ϊ��5V��10-5mol��$\frac{1000mL}{20mL}$����0.01L=0.25V mol/L��
�ʴ�Ϊ�����ȣ�0.25V��
�ۼס����������Ƚϣ����ϴ���Ǽף���Ϊ�÷�Ӧ����ʱ������SO2�����к���ˮ����������ʯ�����յij���SO2���ˮ����������SO2������ƫ��������������Ũ��ƫС��
�ʴ�Ϊ���ף�����ʯ�����յij���SO2���ˮ����������SO2������ƫ�����������Ũ��ƫС��
���� ���⿼��ͭ��Ũ����ķ�Ӧ���������ۡ�ʵ�������������������к͵ζ���ָʾ����ѡ����ȣ��Ƕ�ѧ���ۺ������Ŀ��飬����������ѧ���Ļ�ѧʵ��������������������������

| A�� | ���������ʣ�������к��ʱ���˰����� | |
| B�� | Na2O2��NH4C1��MgCl2�����ں��й��ۼ������ӻ����� | |
| C�� | ��ϩ������ϩ������ͨ���ۺϷ�Ӧ�õ��߷��Ӳ��� | |
| D�� | ������ˮ����ά����Ҫ�ɷֶ��ǹ����� |
| A�� | pH=1����Һ��Na+��NH4+��S2-��NO3- | |
| B�� | c��HSO4-��=0.1 mol/L����Һ��K+��Ba2+��HCO3-��Cl- | |
| C�� | ����������������ɫ����Һ��Na+��K+��I-��SO42- | |
| D�� | ���ܽ�̼��Ƶ���Һ��Na+��NH4+��Cl-��Br- |
| A�� | ��Cl2��MnO2�����ᣨϡ�� | B�� | ��H2�����ᣨϡ����Zn | ||
| C�� | ��O2��MnO2��H2O2 | D�� | ��CO2�����ᣨϡ����CaCO3 |
| A�� | 2000kJ | B�� | ��H=1500kJ/mol | C�� | ��H=-2000kJ/mol | D�� | -3 000kJ/mol |
| A�� | Ũ������ϡ�������ǿ������ | |
| B�� | ijǿ������Һ�к��н϶��SO32-��S2- | |
| C�� | SO2��H2SO3��H2S�����л�ԭ�� | |
| D�� | ��BaCl2��Һ���ɰ�ɫ������ԭ��Һ��һ������SO42- |
��ú��ȼ�� ��ȼ�ű��� �۹�ҵ�������ŷ� ��������β����
| A�� | �٢� | B�� | �ۢ� | C�� | �٢ڢ� | D�� | �٢ڢۢ� |