题目内容
10.FeCl3在现代工业生产中应用广泛.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华.工业上,向500-600℃的铁屑中通入氯气可生产无水氯化铁;向炽热铁屑中通入氯化氢可以生产无水氯化亚铁.某化学研究性学习小组模拟工业生产流程制备无水FeCl3并对产物做了如下探究实验,
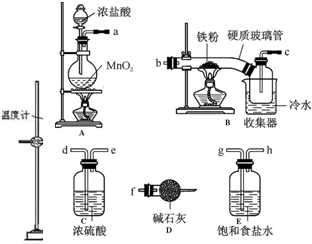
请回答下列问题:
(1)装置的连接顺序为aghdebcf(用a、b、c…h表示).
(2)i.E中饱和食盐水的作用是除去氯气中的氯化氢气体,防止生成FeCl2杂质、防止H2和Cl2混合爆炸.
ii.D中碱石灰的作用是吸收没有反应完的氯气,以防污染空气;吸收空气中的水蒸气,防止生成的FeCl3潮解.
(3)反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端.要使沉积得FeCl3进入收集器,需进行的操作是在沉积的FeCl3固体下方加热.
(4)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:

①淡黄色溶液中加入试剂X生成淡红色溶液的离子方程式为Fe3++3SCN-?Fe(SCN)3.
②淡红色溶液中加入过量H2O2后溶液红色加深的原因是2Fe2++2H++H2O2═2Fe3++2H2O(用离子方程式表示).
(5)已知红色褪去的同时有气体生成,经检验为O2.该小组同学对红色褪去的原因进行探究.
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀.
②另取同物质的量浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化.
实验①说明SCN-发生了反应而不是Fe3+发生反应;
实验②的目的是排除H2O2分解产生的O2氧化SCN-的可能;
得出结论:H2O2将SCN-氧化成SO42-.
分析 (1)排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理,无水FeCl3在空气中易潮解,加热易升华.工业上,向500-600℃的铁屑中通入氯气可生产无水氯化铁;向炽热铁屑中通入氯化氢可以生产无水氯化亚铁.装置A制备氯气,通过装置E中饱和食盐水吸收氯化氢气体,通过装置装置C中的浓硫酸除去水蒸气,通过装置B生成氯化铁后冷却得到固体污水氯化铁,最后需要连接装置D避免空气中水蒸气进入装置B使氯化铁水解;
(2)i.E中饱和食盐水的作用是除去氯气中氯化氢;
ii.D中碱石灰的作用是吸收多余污染气体,防止空气中水蒸气进入装置B;
(3)无水FeCl3在空气中易潮解,加热易升华;
(4)①根据Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈血红色;
②Fe2+被H2O2氧化生成Fe3+,从而增大Fe3+浓度;
(5)根据①滴加FeCl3溶液无明显变化,说明SCN-发生了反应而不是Fe3+发生反应,滴加稀HCl和BaCl2溶液,产生白色沉淀,说明生成了硫酸根;
根据②另取同浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化,说明O2不能氧化SCN-.
解答 解:(1)浓硫酸具有吸水性能作氯气干燥剂、碱石灰具有碱性而吸收氯气、饱和食盐水吸收氯化氢而抑制氯气溶解,装置排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理,所以装置连接顺序为a→g→h→d→e→b→c→f,故答案为:a、g、h、d、e、b、c、f;
(2)i.饱和食盐水吸收氯化氢而抑制氯气溶解,除去氯气中的氯化氢气体,防止生成FeCl2杂质,防止H2和Cl2混合爆炸,
故答案为:除去氯气中的氯化氢气体,防止生成FeCl2杂质、防止H2和Cl2混合爆炸;
ii.D中碱石灰的作用是吸收多余污染气体,防止空气中水蒸气进入装置B,吸收没有反应完的氯气,以防污染空气,吸收空气中的水蒸气,防止生成的FeCl3潮解,
故答案为:吸收没有反应完的氯气,以防污染空气;吸收空气中的水蒸气,防止生成的FeCl3潮解;
(3)无水FeCl3在空气中易潮解,加热易升华,反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端.要使沉积得FeCl3进入收集器,需进行的操作是在沉积的FeCl3固体下方加热,
故答案为:在沉积的FeCl3固体下方加热;
(4)①Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈血红色,反应方程式为Fe3++3SCN-?Fe(SCN)3,
故答案为:Fe3++3SCN-?Fe(SCN)3;
②Fe2+被H2O2氧化生成Fe3+,从而增大Fe3+浓度,Fe3+、SCN-反应生成Fe(SCN)3,从而增大络合物浓度,溶液颜色加深,反应的化学方程式为:2Fe2++2H++H2O2═2Fe3++2H2O,
故答案为:2Fe2++2H++H2O2═2Fe3++2H2O;
(5)根据①滴加FeCl3溶液无明显变化,说明SCN-发生了反应而不是Fe3+发生反应,滴加稀HCl和BaCl2溶液,产生白色沉淀,说明生成了硫酸根;
根据②另取同浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化,说明O2不能氧化SCN-,所以氧化SCN-的为双氧水;
故答案为:SCN-发生了反应而不是Fe3+发生反应;排除H2O2分解产生的O2氧化SCN-的可能;H2O2将SCN-氧化成SO42-.
点评 本题通过探究氯气与铁反应,考查了物质性质实验方案的设计方法,题目难度中等,注意掌握氯气与铁反应的现象、反应原理,明确物质性质实验方案的设计原则,试题充分考查了学生的分析、理解能力及化学实验能力.

 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案| A. | 两种物质反应,不管怎样书写化学方程式,平衡常数不变 | |
| B. | 某温度下,2L密闭容器中加入4mol A和2mol B发生反应: 3A(g)+2B(g)?4C(s)+2D(g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=$\frac{{c}^{4}(C){c}^{2}(D)}{{c}^{3}(A){c}^{2}(B)}$ | |
| C. | 温度一定时,当溶液中c(Ag+)•c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | |
| D. | 难溶电解质AB2饱和溶液中,c(A2+)=x mol•L-1,c(B-)=y mol•L-1,则Ksp值为4xy2 |
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol (燃烧热) | |
| B. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | S(s)+O2(g)═SO2(g)△H=-296.8 kJ/mol (反应热) | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,则△H1>△H2 |
| 化学键 | H-H | N三N | N-H |
| 键能/(kJ•mol-1) | 436 | 945.6 | 391 |
| A. | +192.4 kJ•mol-1 | B. | +92.4kJ•mol-1 | C. | -92.4kJ•mol-1 | D. | -192.4kJ•mol-1 |
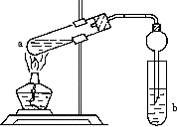 如图,在试管a中先加入2mL95%的乙醇,再加入3mL无水醋酸,边摇边缓缓加入2mL浓H2SO4,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.
如图,在试管a中先加入2mL95%的乙醇,再加入3mL无水醋酸,边摇边缓缓加入2mL浓H2SO4,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.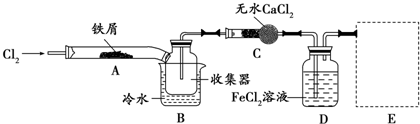
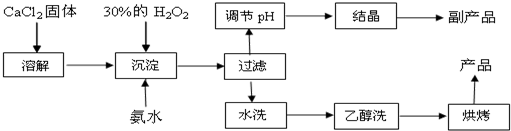
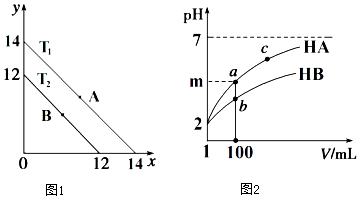 (1)溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图1所示.
(1)溶液中,c(H+)=10-x mol•L-1,c(OH-)=10-y mol•L-1,x与y的关系如图1所示.