题目内容
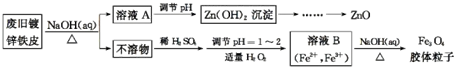
5.纯净的过氧化钙(CaO2)是白色粉末,难溶于水,不溶于乙醇、乙醚,常温下较为稳定,是一种新型水产养殖增氧剂,常用于鲜活水产品的运输.已知:在实验室可用钙盐制取CaO2•8H2O,再经脱水制得CaO2.其制备过程如下: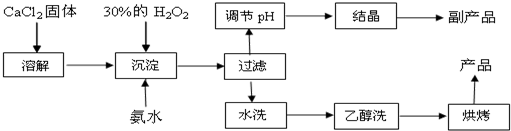
(1)“溶解”过程需要的玻璃仪器有烧杯、玻璃棒;“沉淀”时需控制反应温度在0℃左右,比较简单易行的方法是将反应容器浸入冰水中;为检验“水洗”是否合格,可取少量洗涤液于试管中,再滴加AgNO3溶液(填试剂),无明显现象说明“水洗”合格.
(2)“沉淀”时发生反应的离子方程式为Ca2++2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4+;该制法的副产品为NH4Cl(填化学式);若称取11.1g无水CaCl2,理论上应该量取质量分数30%、密度1.1g/cm3的H2O2溶液10.3mL.
(3)测定产品中CaO2的含量的实验步骤是:
第一步,准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2mol/L的H2SO4溶液,充分反应;
第二步,向上述锥形瓶中加入几滴淀粉溶液;
第三步,逐滴加入浓度为c mol/L的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL.【已知:I2+2S2O32-→2I-+S4O62-(无色)】
①第三步中说明反应恰好完全的现象是溶液由蓝色变为无色,且30s不恢复.
②CaO2的质量分数为$\frac{36cV×10{\;}^{-3}}{a}$ (用字母表示);
③某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能偏高(填“偏高”、“偏低”、“无影响”、“不能确定”)
分析 (1)“溶解”过程需要的玻璃仪器为烧杯、玻璃棒;为了控制沉淀温度为0℃左右,在实验室宜采取的方法是冰水浴冷却可以达到实验目的;根据检验水洗后没有Cl-离子的方法判断合格;
(2)实验的目的为制备CaO2•8H2O,则流程中的沉淀应为CaO2•8H2O,根据质量守恒判断还应有NH4Cl生成,根据质量守恒定律可写出反应的离子方程式;由方程式得n(H2O2)=n(CaCl2)计算;
(3))①CaO2具有强氧化性,溶液中加入KI晶体和淀粉溶液,生成的碘单质遇淀粉变蓝色,据此分析;
②根据反应的离子方程式,CaO2+4H++2I-═Ca2++2H2O+I2,I2+2S2O32-→2I-+S4O62-,可得关系式CaO2~2S2O32-,并以此进行计算;
③根据空气中的氧气能够氧化碘离子,使碘单质的量增加,消耗的硫代硫酸钠增加分析.
解答 解:(1)“溶解”过程需要的玻璃仪器为烧杯、玻璃棒;为了控制沉淀温度为0℃左右,在实验室宜采取的方法是冰水浴冷却可以达到实验目的,比较简单易行的方法是将反应容器浸入冰水中;为检验“水洗”是否合格,检验水洗后没有Cl-离子即可,则可取少量洗涤液于试管中,再滴加 AgNO3溶液,无明显现象说明“水洗”合格;故答案为:烧杯、玻璃棒;将反应容器浸入冰水中;AgNO3溶液;
(2)本实验的目的为制备CaO2•8H2O,则流程中的沉淀应为CaO2•8H2O,根据质量守恒判断还应有NH4Cl生成,故反应的离子方程式为:Ca2++2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4+;副产品为NH4Cl;
由方程式得n(H2O2)=n(CaCl2),所以设量取质量分数30%、密度1.1g/cm3的H2O2溶液xmL,则有$\frac{11.1g}{111g/mol}$=$\frac{1.1x×30%g}{34g/mol}$,解得x=10.3ml
故答案为:Ca2++2NH3•H2O+H2O2+6H2O=CaO2•8H2O↓+2NH4+;NH4Cl;10.3;
(3)①CaO2具有强氧化性,溶液中加入KI晶体和淀粉溶液,生成的碘单质遇淀粉变蓝色,反应的离子方程式为:CaO2+4H++2I-═Ca2++2H2O+I2,所以反应恰好完全的现象是溶液由蓝色变为无色,且30s不恢复,故答案为:溶液由蓝色变为无色,且30s不恢复;
②根据反应的离子方程式,CaO2+4H++2I-═Ca2++2H2O+I2,I2+2S2O32-→2I-+S4O62-,可得关系式并以此进行计算:
CaO2~2S2O32-
72g 2mol
m cV×10-3mol
m=$\frac{72g×cV×10-3mol}{2mol}$=36cV×10-3g
则CaO2的质量分数为$\frac{36cV×10{\;}^{-3}}{a}$
故答案为:$\frac{36cV×10{\;}^{-3}}{a}$;
③在酸性条件下空气中的O2也可以把KI氧化为I2,使消耗的Na2S2O3增多,从而使测得的CaO2的质量分数偏高,
故答案为:偏高;在酸性条件下空气中的O2也可以把KI氧化为I2,使消耗的Na2S2O3增多,从而使测得的CaO2的质量分数偏高
点评 本题考查形式为物质制备流程图题目,涉及物质的化学方程式的书写,实验方法和实验操作、物质的检验和计算等问题,做题时注意分析体重关键信息,掌握实验基本操作等问题,本题较为综合.

 教材全解字词句篇系列答案
教材全解字词句篇系列答案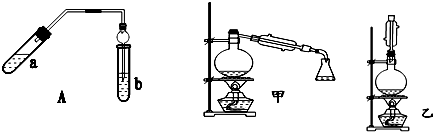
请回答下列问题:
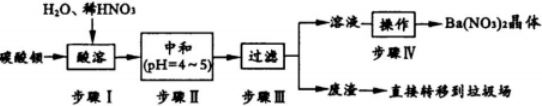
(1)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑.
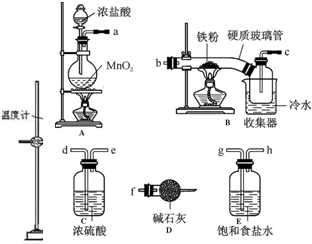
(2)A装置中使用球形管除起到冷凝作用外,另一重要作用是防止倒吸,步骤⑤中分离乙酸乙酯必须使用的一种仪器是分液漏斗.
(3)为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图A所示装置进行了以下4个实验.实验开始先用酒精灯微热3min,再加热使之微微沸腾3min.实验结束后充分振荡小试管b再测有机层的厚度,实验记录如下:
| 实验编号 | 试管a中试剂 | 试管b中试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL18mol•L-1 浓硫酸 | 饱和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
②分析实验AC(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率.浓硫酸的吸水性能够提高乙酸乙酯产率的原因是浓硫酸可以吸收酯化反应中生成的水,降低了生成物浓度使平衡向生成乙酸乙酯的方向移动.
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是大量乙酸、乙醇未经反应就脱离反应体系;温度过高发生其他反应.
④分离出乙酸乙酯层后,经过洗涤杂质;为了干燥乙酸乙酯可选用的干燥剂为(填字母)B.
A.P2O5 B.无水Na2SO4 C.碱石灰 D.NaOH固体
⑤为充分利用反应物,该同学又设计了图中甲、乙两个装置(利用乙装置时,待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物).你认为更合理的是乙.理由是:乙装置能将易挥发的反应物乙酸和乙醇冷凝回流到反应容器中,继续反应,提高了乙酸、乙醇原料的利用率及产物的产率,而甲不可.