题目内容
下列各图所表示的反应属于放出热量的是( )
A、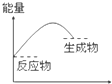 |
B、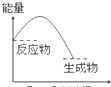 |
C、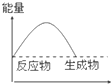 |
D、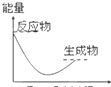 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:反应物的总能量大于生成物的总能量为放热反应,反应物的总能量小于生成物的总能量为吸热反应,据此判断.
解答:
解:A.图象中反应物的总能量小于生成物的总能量为吸热反应,故A不选;
B.图象中反应物的总能量大于生成物的总能量为放热反应,符合题意,故B选;
C.反应物的总能量等于生成物的总能量为放热反应,不存在这种情况,故C错误;
D.反应物断键时要吸收能量,所以反应物的能量先升高,图象不符合,图象错误,故D错误.
故选B.
B.图象中反应物的总能量大于生成物的总能量为放热反应,符合题意,故B选;
C.反应物的总能量等于生成物的总能量为放热反应,不存在这种情况,故C错误;
D.反应物断键时要吸收能量,所以反应物的能量先升高,图象不符合,图象错误,故D错误.
故选B.
点评:本题考查了化学反应中的能量变化图,侧重于吸热反应和放热反应的判断的考查,题目难度不大.

练习册系列答案
相关题目
SO2 气体通入BaCl2 无沉淀产生,但分别加入①NH3?H2O 水 ②氯水 ③H2S 溶液三种溶液均有沉淀产生这些沉淀分别为( )
| A、BaSO4、BaSO3、S |
| B、S、BaSO3、BaSO4 |
| C、BaSO3、BaSO4、S |
| D、BaSO3、S、BaSO4 |
能正确表示下列反应的离子方程式是( )
| A、少量金属钠放入冷水中 Na+2H2O=Na++2OH-+H2↑ |
| B、水溶液中NaHCO3的电离:HCO3-?CO32-+H+ |
| C、碳酸氢铵溶液和氢氧化钠溶液等物质的量浓度、等体积混合 NH4++OH-═NH3?H2O |
| D、硫酸铜溶液和氢氧化钡溶液混合 Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓ |
下列过程一定不能自发进行的是( )
| A、4NO2(g)+O2(g)=2N2O5(g);△H<0 |
| B、2CO(g)=2C(s)+O2(g);△H>0 |
| C、(NH4)2CO3(s)=NH4HCO3(s)+NH3(g);△H>0 |
| D、2H2(g)+O2(g)=2H2O(l);△H<0 |
向氢氧化铁溶胶中逐滴加入一种液体,首先使溶胶发生凝聚而沉淀,继续加入使沉淀消失,这种液体是( )
| A、蒸馏水 |
| B、0.5 mol?L-1硫酸镁溶液 |
| C、0.5 mol?L-1氯化钾溶液 |
| D、0.5 mol?L-1盐酸 |
下列叙述不正确的是( )
| A、标准状况下,1 mol任何气体体积均约为22.4 L |
| B、同温、同压下,体积相同的两种气体单质具有相同的分子数目 |
| C、将73 g HCl溶于1 L水中配成溶液,所得溶液物质的量浓度是2 mol?L-1 |
| D、含NA个Na+的Na2O溶解于水配成1 L溶液,Na+的物质的量浓度为1 mol?L-1 |
