题目内容
SO2 气体通入BaCl2 无沉淀产生,但分别加入①NH3?H2O 水 ②氯水 ③H2S 溶液三种溶液均有沉淀产生这些沉淀分别为( )
| A、BaSO4、BaSO3、S |
| B、S、BaSO3、BaSO4 |
| C、BaSO3、BaSO4、S |
| D、BaSO3、S、BaSO4 |
考点:二氧化硫的化学性质
专题:
分析:将SO2气体通入BaCl2溶液无沉淀生成,因盐酸酸性大于亚硫酸的酸性,二者不反应,若通入气体生成沉淀,则发生氧化还原反应生成硫酸根离子或增大二氧化硫的溶解度生成亚硫酸盐,以此来解答.
解答:
解:将SO2气体通入BaCl2溶液无沉淀生成,因盐酸酸性大于亚硫酸的酸性,二者不反应,
①NH3有沉淀生成,是因二氧化硫与氨气生成亚硫酸根离子与钡离子结合生成亚硫酸钡沉淀,
②Cl2水有沉淀生成,是因发生氧化还原反应生成硫酸根离子与钡离子结合生成硫酸钡沉淀;
③H2S有沉淀,是因二氧化硫与硫化氢发生氧化还原反应生成S;
故选C.
①NH3有沉淀生成,是因二氧化硫与氨气生成亚硫酸根离子与钡离子结合生成亚硫酸钡沉淀,
②Cl2水有沉淀生成,是因发生氧化还原反应生成硫酸根离子与钡离子结合生成硫酸钡沉淀;
③H2S有沉淀,是因二氧化硫与硫化氢发生氧化还原反应生成S;
故选C.
点评:本题考查二氧化硫的性质,为高频考点,把握发生的反应确定沉淀的成分为解答的关键,侧重氧化还原反应及复分解反应的考查,注意酸性的比较,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列除去杂质的方法中错误的是( )
| 物质 | 杂质 | 除杂质的方法 | |
| A | CaCl2溶液 | HCl | 过量CaCO3、过滤 |
| B | KNO3溶液 | AgNO3 | 过量NaCl溶液、过滤 |
| C | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D | CO2 | H2O | 通过盛浓硫酸的洗气瓶 |
| A、A | B、B | C、C | D、D |
下列有关物质的说法正确的是( )
| A、根据红外光谱图的分析可以初步判断有机物中具有哪些基团 |
| B、邻二甲苯有两种空间结构 |
| C、“神州七号”的防护层中含聚四氟乙烯,聚四氟乙烯属于不饱和烃 |
| D、油脂是一类高分子化合物,是高级脂肪酸甘油酯 |
在4NH3+5O2?4NO+6H2O反应中,表示该反应速率最快的是( )
| A、υ(NH3)=0.8mol/(L?s) |
| B、υ(O2)=1.0mol/(L?s) |
| C、υ(NO)=1.0mol/(L?s) |
| D、υ(H2O)=1.8mol/(L?s) |
下表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ):
根据上述数据回答下列物质本身具有的能量最低的是( )
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
| A、Cl2 |
| B、Br2 |
| C、I2 |
| D、H2 |
120℃、101kPa,甲烷(CH4)和过量的O2的混合物,用电火花引燃(CH4+2O2=CO2+2H2O)后,恢复到原来的温度和压强,测得反应后气体密度为相同条件下H2密度的15倍,则原混合气体中甲烷和氧气的体积比为( )
| A、9:1 | B、1:9 |
| C、1:7 | D、7:1 |
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、25℃和101KPa的条件下,4.9LCH4完全燃烧生成的H2O的分子数为0.4NA |
| B、1molNH3中含有3NA对电子对 |
| C、Na2O2与H2O反应生成标准状况下11.2 L O2时,转移的电子数为2NA |
| D、标准状况下,2.24L HF中所含电子数为NA |
下列各图所表示的反应属于放出热量的是( )
A、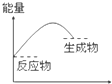 |
B、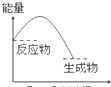 |
C、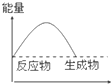 |
D、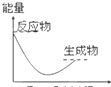 |