题目内容
下列有关实验的说法正确的是( )
| A、若要除去苯中的苯酚,加入NaOH溶液充分振荡,然后分液 |
| B、向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体现象,说明溶液中的反应生成了NO2 |
| C、向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2浊液,加热,没有红色沉淀生成,说明淀粉没有水解成葡萄糖 |
| D、相同温度下,取两份等质量的锌粒分别与足量稀硫酸反应,向其中一份中加入几滴CuSO4溶液.加入CuSO4溶液的产生氢气快,最终二者生成氢气的量相同 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.苯酚与NaOH溶液反应,生成苯酚钠和水,苯与NaOH溶液反应不反应;
B.NO3-在酸性条件下具有氧化性,被还原生成NO,NO被O2氧化为红棕色的NO2;
C.淀粉水解生成葡萄糖,葡萄糖与氢氧化铜浊液应在碱性条件下反应;
D.锌和硫酸铜反应生成铜,锌铜在硫酸中形成原电池反应加快反应速率,但生成氢气量减少.
B.NO3-在酸性条件下具有氧化性,被还原生成NO,NO被O2氧化为红棕色的NO2;
C.淀粉水解生成葡萄糖,葡萄糖与氢氧化铜浊液应在碱性条件下反应;
D.锌和硫酸铜反应生成铜,锌铜在硫酸中形成原电池反应加快反应速率,但生成氢气量减少.
解答:
解:A.苯酚与NaOH溶液反应,生成苯酚钠和水,苯与NaOH溶液反应不反应,溶液分层,分液即可得到纯净的苯,故A正确;
B.向Fe(NO3)2溶液中加入H2SO4,则会发生离子反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,产生的NO在管口生成NO2呈现红色,而不是HNO3分解产生NO2,故B错误;
C.淀粉在酸性条件下水解生成葡萄糖,葡萄糖与氢氧化铜浊液应在碱性条件下反应,反应后的溶液应先加入氢氧化钠溶液调节溶液至碱性,故C错误;
D.滴加过 CuSO4溶液的样品由于一部分锌置换了CuSO4中的铜,形成原电池,使反应速率加快,但产生氢气的量减少,故D错误.
故选A.
B.向Fe(NO3)2溶液中加入H2SO4,则会发生离子反应:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,产生的NO在管口生成NO2呈现红色,而不是HNO3分解产生NO2,故B错误;
C.淀粉在酸性条件下水解生成葡萄糖,葡萄糖与氢氧化铜浊液应在碱性条件下反应,反应后的溶液应先加入氢氧化钠溶液调节溶液至碱性,故C错误;
D.滴加过 CuSO4溶液的样品由于一部分锌置换了CuSO4中的铜,形成原电池,使反应速率加快,但产生氢气的量减少,故D错误.
故选A.
点评:本题考查较为综合,涉及物质的性质、分离提纯、化学反应速率等知识,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
下列叙述正确的是( )
| A、常温下,向AgCl的饱和溶液中加入NaCl固体,有固体析出,且AgCl的Ksp变小 |
| B、10 mL 0.02 mol?L-1 HCl溶液与10 mL 0.02 mol?L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 |
| C、在0.1 mol?L-1 CH3COONa溶液中,c(OH-)>c(CH3COOH)+c(H+) |
| D、0.1 mol?L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
已知25℃时,AgI饱和溶液中c(Ag+)为1.22×10-8mol/L,AgCl的饱和溶液中c(Ag+)为1.30×10-5mol/L.若在5mL含有KCl和KI浓度均为0.01mol/L的混合溶液中,滴加8mL 0.01mol/L的AgNO3溶液,则下列叙述中不正确的是A( )
| A、反应后溶液中离子浓度大小关系为:c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| B、发生反应生成的AgI沉淀多于AgCl沉淀 |
| C、在水中AgCl的溶解度比AgI的溶解度大 |
| D、若在AgCl悬浊液中滴加KI溶液,白色沉淀会转变成黄色沉淀 |
下列说法正确的是( )
| A、在晶体中只要有阳离子就一定有阴离子 |
| B、加热至沸腾蒸发水分时,溶液的浓度一定增大 |
| C、一个原子或单核离子,最外层有8个电子时,一定达到了稳定结构 |
| D、水的分子量不到空气平均分子量的2/3,如果水分子间没有特殊的作用力,地球上就不会有液态水 |
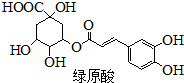 绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )
绿原酸是一种有降压作用的药物,可由咖啡酸(一种芳香酸)与奎尼酸通过酯化反应合成.下列说法正确的是( )| A、奎尼酸分子式为C7H14O6 |
| B、绿原酸能发生取代、加成、消去和缩聚反应 |
| C、1mol奎尼酸与NaOH溶液反应,最多消耗5molNaOH |
| D、咖啡酸和奎尼酸都能与FeCl3溶液发生显色反应 |
化学式为C16H23Cl3O2的有机物分子内不含有碳碳叁键,它所含的双键数目最多是( )
| A、5 | B、4 | C、3 | D、2 |
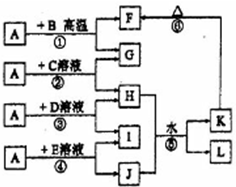 如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答: