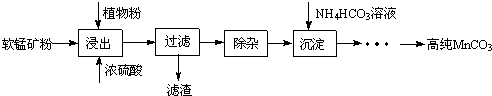
题目内容
20.砹是第七主族第六周期的元素,推测砹或砹的化合物最不可能具有的性质是( )| A. | HAt很稳定 | B. | 砹易溶于某些有机溶剂 | ||
| C. | AgAt不溶于水 | D. | 砹是有色固体 |
分析 砹是原子序数最大的卤族元素,利用ⅤⅡA元素性质的相似性和递变性来解答,
A.同主族从上到下非金属性减弱,气态氢化物稳定性减弱;
B.同主族元素单质的性质相似;
C.同主族元素化合物的性质相似;
D.同主族从上到下元素的单质从气态、液态、固态变化,且颜色加深.
解答 解:A.同主族从上到下元素非金属性逐渐减弱,对应的氢化物也在减弱,所以HAt很不稳定,故A错误;
B.碘易溶于有机溶剂,同主族元素单质的性质相似,则砹易溶于某些有机溶剂,故B正确;
C.因AgCl不溶于水,同主族元素的化合物的性质相似,则AgAt不溶于水,故C正确;
D.同主族从上到下元素的单质从气态、液态、固态变化,且颜色加深,则砹是有色固体,故D正确;
故选:A.
点评 本题考查元素周期律,题目较简单,熟悉第ⅤⅡA族元素的性质变化规律即可解答.

练习册系列答案
相关题目
10.用布氏漏斗和吸滤瓶接抽水泵过滤沉淀后,正确的操作是( )
| A. | 先关水龙头,拔下抽滤瓶上的橡皮管,再取下布氏漏斗 | |
| B. | 先取下布氏漏斗,再关上水龙头 | |
| C. | 先将沉淀和滤纸一起取出,再关上水龙头 | |
| D. | 先拔下抽滤瓶上的橡皮管,关上水龙头,再取下布氏漏斗 |
11.酸碱质子理论的要点是:凡能给出质子(即H+)的分子或离子都是酸;凡能接受质子的分子或离子都是碱.按此观点,下列微粒既属于酸又属于碱的是( )
①H2O ②CO32-③Al3+ ④CH3COOH ⑤NH4+ ⑥HCO3-.
①H2O ②CO32-③Al3+ ④CH3COOH ⑤NH4+ ⑥HCO3-.
| A. | ②③ | B. | ①⑥ | C. | ④⑥ | D. | ⑤⑥ |
8.不同元素的原子电负性不同,若用x值来表示,x值越大,其原子的电负性就越大,吸引电子的能力越强,在所形成的分子中成为带负电荷的一方,下面是某些短周期元素的电负性的值:
(1)通过分析x值的变化规律,确定N、Mg的x值的范围:0.93<x(Mg)<1.57,2.55<x(N)<3.44.
(2)推测x值与原子半径的关系是同周期(或同主族)元素,x值越大,原子半径越小.根据短周期元素x值变化特点,体现了元素性质的周期性变化规律.
(3)某有机物结构简式如图,其中C-N中,你认为共用电子对偏向氮原子(填原子名称).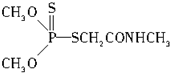
(4)经验规律告诉我们,当成键的两原子的x差值,即△x>1.7时,一般为离子键,当△x<1.7时,一般为共价键.试推断AlBr3中化学键的类型为共价键
(5)预测元素周期表中x值最小的元素是Cs(填元素符号,放射性元素除外).
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 第二周期 | Li | Be | B | C | N | O | F |
| 电负性值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | |
| 第三周期 | Na | Mg | Al | Si | P | S | Cl |
| 电负性值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(2)推测x值与原子半径的关系是同周期(或同主族)元素,x值越大,原子半径越小.根据短周期元素x值变化特点,体现了元素性质的周期性变化规律.
(3)某有机物结构简式如图,其中C-N中,你认为共用电子对偏向氮原子(填原子名称).
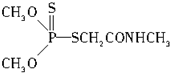
(4)经验规律告诉我们,当成键的两原子的x差值,即△x>1.7时,一般为离子键,当△x<1.7时,一般为共价键.试推断AlBr3中化学键的类型为共价键
(5)预测元素周期表中x值最小的元素是Cs(填元素符号,放射性元素除外).
15.下列关于Cs描述中,错误的是( )
| A. | CsOH是一种既可与强酸又可与强碱反应的两性氢氧化物 | |
| B. | Cs在空气中燃烧可生成Cs2O和Cs2O2 | |
| C. | Cs与水反应,能发生爆炸,并放出H2 | |
| D. | CsOH很稳定,加热不易分解 |
12.取m g AgNO3固体粉末充分加热,得到a L气体和b g固体,将气体用足量的水吸收,剩余气体的体积为c L(气体体积均为同温同压下测定),下列结论一定正确的是( )
| A. | aL气体的平均相对分子质数为41.3 | |
| B. | aL气体被水吸收时转移电子的物质的量为($\frac{2m}{170}-\frac{b}{108}$)mol | |
| C. | cL剩余气体是O2,且c=$\frac{a}{4}$ | |
| D. | 将mgAgNO3溶于水,再加足量的盐酸,$\frac{b}{108}$×143.5g可生成沉淀 |
9.下列关于化学反应速率的说法,正确的是( )
| A. | 化学反应速率通常用单位时间内反应物或生成物的质量变化来表示 | |
| B. | 用不同物质的浓度变化表示同一时间内、同一反应的速率时,其数值之比等于反应方程式中对应物质的化学计量数之比 | |
| C. | 反应速率越大,则单位时间内生成物的产量就越大 | |
| D. | 在反应过程中,反应物浓度逐渐变小,所以用反应物表示的化学反应速率为负值 |
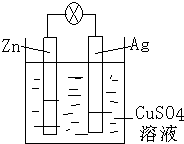 如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液,回答下列问题:
如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液,回答下列问题: