题目内容
将含有2molKAl(SO4)2的溶液和含有3.5molBa(OH)2的溶液混合,则下列说法正确的是( )
| A、反应后溶液呈碱性,且溶液中OH-的物质的量为1mol |
| B、反应后,铝元素的存在形式有Al(OH)3和AlO2-,且物质的量分别为1mol、0.5mol |
| C、反应后溶液中有K2SO4和KAlO2两种溶质 |
| D、反应中生产沉淀Al(OH)3和BaSO4的物质的量分别为2mol、3.5mol |
考点:化学方程式的有关计算
专题:计算题
分析:发生反应:2KAl(SO4)2+3Ba(OH)2=K2SO4+2Al(OH)3↓+3BaSO4↓,2molKAl(SO4)2消耗3molBa(OH)2,剩余0.5mol Ba(OH)2,生成2mol Al(OH)3,2mol K2SO4;
再发生反应:K2SO4+Ba(OH)2=BaSO4↓+2KOH,0.5mol Ba(OH)2反应可以消耗0.5mol K2SO4,生成1mol KOH,剩余0.5mol K2SO4;
还发生反应:Al(OH)3+KOH=KAlO2+2H2O,1mol KOH反应可以消耗1mol Al(OH)3,生成1mol KAlO2,故最终沉淀为1mol Al(OH)3、3.5mol BaSO4,据此解答.
再发生反应:K2SO4+Ba(OH)2=BaSO4↓+2KOH,0.5mol Ba(OH)2反应可以消耗0.5mol K2SO4,生成1mol KOH,剩余0.5mol K2SO4;
还发生反应:Al(OH)3+KOH=KAlO2+2H2O,1mol KOH反应可以消耗1mol Al(OH)3,生成1mol KAlO2,故最终沉淀为1mol Al(OH)3、3.5mol BaSO4,据此解答.
解答:
解:发生反应:2KAl(SO4)2+3Ba(OH)2=K2SO4+2Al(OH)3↓+3BaSO4↓,2molKAl(SO4)2消耗3molBa(OH)2,剩余0.5mol Ba(OH)2,生成2mol Al(OH)3,2mol K2SO4;
再发生反应:K2SO4+Ba(OH)2=BaSO4↓+2KOH,0.5mol Ba(OH)2反应可以消耗0.5mol K2SO4,生成1mol KOH,剩余0.5mol K2SO4;
还发生反应:Al(OH)3+KOH=KAlO2+2H2O,1mol KOH反应可以消耗1mol Al(OH)3,生成1mol KAlO2,故最终沉淀为1mol Al(OH)3、3.5mol BaSO4,
A.由上述分析可知,反应后溶液溶质为K2SO4、KAlO2,氢氧化钠完全反应,偏铝酸根水解,溶液呈碱性,溶液中OH-的物质的量远小于1mol,故A错误;
B.由上述分析可知,反应后,铝元素的存在形式有Al(OH)3和AlO2-,物质的量分别为1mol、1mol,故B错误;
C.由上述分析可知,反应后溶液溶质为K2SO4、KAlO2,故C正确;
D.反应中生产沉淀Al(OH)3和BaSO4的物质的量分别为1mol、3.5mol,故D错误;
故选C.
再发生反应:K2SO4+Ba(OH)2=BaSO4↓+2KOH,0.5mol Ba(OH)2反应可以消耗0.5mol K2SO4,生成1mol KOH,剩余0.5mol K2SO4;
还发生反应:Al(OH)3+KOH=KAlO2+2H2O,1mol KOH反应可以消耗1mol Al(OH)3,生成1mol KAlO2,故最终沉淀为1mol Al(OH)3、3.5mol BaSO4,
A.由上述分析可知,反应后溶液溶质为K2SO4、KAlO2,氢氧化钠完全反应,偏铝酸根水解,溶液呈碱性,溶液中OH-的物质的量远小于1mol,故A错误;
B.由上述分析可知,反应后,铝元素的存在形式有Al(OH)3和AlO2-,物质的量分别为1mol、1mol,故B错误;
C.由上述分析可知,反应后溶液溶质为K2SO4、KAlO2,故C正确;
D.反应中生产沉淀Al(OH)3和BaSO4的物质的量分别为1mol、3.5mol,故D错误;
故选C.
点评:本题考查方程式有关计算、混合物计算等,难度中等,综合考查学生分析和解决问题的能力,明确发生的反应,把握量的关系分析沉淀量的变化为解答的关键,题目难度中等.

练习册系列答案
相关题目
露置的苛性钾经分析含H2O:7.62%,K2CO3:2.38%,KOH:90%,将此样品1g放入1mol?L-1盐酸46mL中,过量的酸用1.070mol?L-1 KOH中和至中性,蒸发中和后的溶液可得固体( )
| A、4.00g | B、3.43g |
| C、4.50g | D、无法计算 |
将H2通过10gCuO粉末加热片刻,冷却后剩余固体的质量为8.4g,那么下列计算正确是( )
| A、有1.6g H2O生成 |
| B、有8.4g Cu生成 |
| C、有80%的CuO被还原 |
| D、实验过程中所消耗的氢气为0.2g |
乙醛和乙炔(C2H2)的混合气体a L,在足量氧气中充分燃烧,同温同压下,消耗氧气的体积为( )
| A、2aL | B、2.5aL |
| C、3aL | D、3.5aL |
海藻中含丰富的、以离子形式存在的碘元素.如图是实验室从海藻里提取碘的流程的一部分下列判断正确的是( )
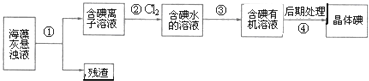

| A、可用淀粉溶液检验步骤②的反应是否进行完全 |
| B、步骤③中加入的有机溶剂是乙醇 |
| C、步骤④的操作是过滤 |
| D、步骤①、③的操作分别是过滤、萃取分液 |