题目内容
12.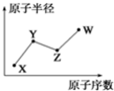 W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.己知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1,下列说法正确的是( )
W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.己知Y、Z两种元素的单质是空气的主要成分,W原子的最外层电子数与Ne原子的最外层电子数相差1,下列说法正确的是( )| A. | Y、Z、W处于同一周期 | |
| B. | X、Y、Z三种元素形成的化合物均为强酸 | |
| C. | Y的氢化物可用于检验W的单质是否泄漏 | |
| D. | 如W的单质泄漏,可以用湿毛巾蘸Y的氢化物的水溶液逃生 |
分析 X、Y、Z、W是四种常见的短周期元素,Y、Z两种元素的单质是空气的主要成分,Z的原子序数大于Y,可推知Z为O、Y为N,W原子的最外层电子数与Ne原子的最外层电子数相差1,则W最外层电子数为7,原子半径大于O原子半径,故W为Cl元素;X的原子序数小于N元素,而原子半径小于N原子,故X为H元素,结合元素化合物性质解答.
解答 解:X、Y、Z、W是四种常见的短周期元素,Y、Z两种元素的单质是空气的主要成分,Z的原子序数大于Y,可推知Z为O、Y为N,W原子的最外层电子数与Ne原子的最外层电子数相差1,则W最外层电子数为7,原子半径大于O原子半径,故W为Cl元素;X的原子序数小于N元素,而原子半径小于N原子,故X为H元素,
A.Y为N,Z为O,二者处于第二周期,W为Cl,处于第三周期,故A错误;
B.X、Z、W形成的化合物中HClO为弱酸,故B错误;
C.氨气与氯气反应会生成氯化铵,可以用于检验氯气泄漏,故C正确;
D.氨水易挥发,氨气具有刺激性,氯气泄漏不能用湿毛巾蘸氨水逃生,故D错误.
故选:C.
点评 本题考查位置结构性质关系等,难度中等,推断元素是解题的关键,注意对元素周期律的理解与运用.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
2.下列热化学方程式表达正确的是(△H的绝对值均正确)( )
| A. | C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol(燃烧热) | |
| B. | S(s)+O2(g)=SO2(g)△H=-269.8kJ/mol (反应热) | |
| C. | NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1)△H=+57.3kJ/mol(中和热) | |
| D. | 2NO2=O2+2NO△H=+116.2kJ/mol (反应热) |
3.下列说法正确的是( )
| A. | 甘油(CH2OH-CHOH-CH2OH)分子中含有1个手性碳原子 | |
| B. | 互为手性异构体的化合物,所含化学键的种类和数目完全相同 | |
| C. | 互为手性异构体的化合物,在三维空间不能重合,但物理、化学性质却几乎完全相同 | |
| D. | 互为手性异构体的化合物,分子组成不同,所以物理、化学性质也不同 |
20.下列反应既属于氧化还原反应,又是吸热反应的是( )
| A. | 锌粒与稀硫酸的反应 | |
| B. | 水分解生成氢气和氧气 | |
| C. | 甲烷在空气中燃烧的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
17.化学科学需要借助化学专用语言来描述,下列有关化学用语不正确的是( )
| A. | 甲烷分子的球棍模型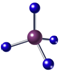 | |
| B. | Cl-的结构示意图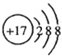 | |
| C. | 中子数为8的碳原子的核素符号为12C | |
| D. | 中子数为1的氢原子的核素符号为21H |
4.下列对碱金属性质的叙述中,正确的是( )
| A. | 都是银白色的柔软金属,密度都比水小 | |
| B. | 单质在空气中燃烧生成的都是过氧化物 | |
| C. | 碱金属单质都能与盐酸反应放出氢气 | |
| D. | 单质的熔、沸点随着原子序数的增加而升高 |
1.已知某元素M原子的最外层电子排布式为nS1,下列说法正确的是( )
| A. | M一定是金属元素 | B. | M一定是S区元素 | C. | M的最高价是+1价 | D. | M可能呈现出-1价 |