题目内容
1.下列各组微粒在水溶液中大量共存的是( )| A. | Na+、I-、K+、Br2 | B. | Mg2+、Cu2+、SO42-、NO3- | ||
| C. | Fe2+、Cl2、K+、SO42- | D. | ClO-、Cl-、CO2、Na+ |
分析 根据离子之间不能结合生成水、气体、沉淀等,不能发生氧化还原反应,则离子能大量共存,以此来解答.
解答 解:A.I-、Br2发生氧化还原反应而不能大量共存,故A错误;
B.该组离子之间不反应,能大量共存,故B正确;
C.Fe2+、Cl2发生氧化还原反应而不能大量共存,故C错误;
D.ClO-、CO2在溶液中反应生成HClO,不能电大量共存,故D错误.
故选B.
点评 本题考查离子的共存,为高考高频考点,侧重考查学生的分析能力,注意把握物质的性质,注意基础知识的考查,题目难度不大.

练习册系列答案
 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
9.氮及其化合物在工农业生产、生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-l
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-l
2C(s)+O 2(g)=2CO(g)△H=-221kJ•mol-l
若某反应的平衡常数表达式为:k=$\frac{c({N}_{2})•{c}^{2}(C{O}_{2})}{{c}^{2}(NO)•{c}^{2}(CO)}$,请写出此反应的热化学方程式2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5kJ•molˉ1.
(2)N2O5在一定条件下可发生分解:2N2O5(g)?4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
①反应开始时体系压强为P0,第3.00min时体系压强为p1,则p1:p0=1.975;2.00min~5.00min内,O2的平均反应速率为0.055mol•Lˉ1•minˉ1.
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是a.
a.容器中压强不再变化
b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5)
d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O 4与NO2之间存在反应:N2O4(g)?2NO2(g)△H=QkJ•mol-1.将一定量的NO放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图1所示.
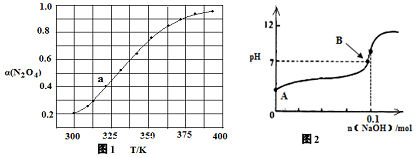
如图1中a点对应温度下,已知N2O4的起始压强p0为200kPa,该温度下反应的平衡常数Kp=213.3KPa(小数点后保留一位数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(4)将固体氢氧化钠投入0.1mol/L的HN3(氢叠氮酸)溶液当中,溶液的体积1L(溶液体积变化忽略不计)溶液的pH变化如图2所示,HN3的电离平衡常数K=1×10-5,B点时溶液的pH=7,计算B点时加入氢氧化钠的物质的量0.099mol(保留两位有效数字).
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ•mol-l
C(s)+O2(g)=CO2(g)△H=-393.5kJ•mol-l
2C(s)+O 2(g)=2CO(g)△H=-221kJ•mol-l
若某反应的平衡常数表达式为:k=$\frac{c({N}_{2})•{c}^{2}(C{O}_{2})}{{c}^{2}(NO)•{c}^{2}(CO)}$,请写出此反应的热化学方程式2NO(g)+2CO(g)?N2(g)+2CO2(g)△H=-746.5kJ•molˉ1.
(2)N2O5在一定条件下可发生分解:2N2O5(g)?4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/(mol•L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是a.
a.容器中压强不再变化
b.NO2和O2的体积比保持不变
c.2v正(NO2)=v逆(N2O5)
d.气体的平均相对分子质量为43.2,且保持不变
(3)N2O 4与NO2之间存在反应:N2O4(g)?2NO2(g)△H=QkJ•mol-1.将一定量的NO放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如图1所示.

如图1中a点对应温度下,已知N2O4的起始压强p0为200kPa,该温度下反应的平衡常数Kp=213.3KPa(小数点后保留一位数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
(4)将固体氢氧化钠投入0.1mol/L的HN3(氢叠氮酸)溶液当中,溶液的体积1L(溶液体积变化忽略不计)溶液的pH变化如图2所示,HN3的电离平衡常数K=1×10-5,B点时溶液的pH=7,计算B点时加入氢氧化钠的物质的量0.099mol(保留两位有效数字).
16.下列物质属于氧化物的是( )
| A. | Cl2O | B. | H2SO4 | C. | C2H5OH | D. | KNO3 |
6.下列反应的离子方程式正确的是( )
| A. | 制作印刷电路板:Fe3++Cu═Cu2++Fe2+ | |
| B. | 等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | Ca(OH)2溶液与足量Ca(HCO3)2溶液反应:Ca2++2HCO3-+2OH-═2CaCO3↓+2H2O+CO32- | |
| D. | 新制饱和氯水中加入石灰石可提高溶液中HClO浓度:CaCO3+2Cl2+H2O═Ca2++2Cl-+CO2↑+2H2O |
13.下列说法中,不正确的是( )
| A. | 碘单质升华,克服的是其分子间作用力 | |
| B. | 金刚石、石墨、纳米碳管是碳元素的同素异形体 | |
| C. | 目前科学家还无法实现对原子或分子的操纵 | |
| D. | HCl气体溶于水后,共价键被破坏,从而形成了H+和Cl- |
10.据报道:研究人员破解了北京及华北地区雾霾主要成分硫酸盐的形成之谜,发现在大气细颗粒物吸附的水分中NO2与SO2的化学反应是当前雾霾期间硫酸盐的主要生成路径.某实验小组对NO2和SO2的反应进行探究.
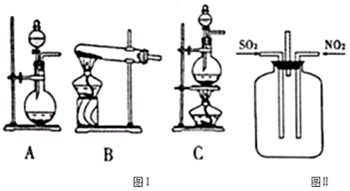
(1)SO2的发生装置可以选择图Ⅰ中的A(或C )(填字母),反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O[或Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O].
(2)按图Ⅱ所示进行实验.
①实验时往集气瓶中通入等体积的SO2和NO2,观察到集气瓶中有白烟产生,通入的NO2气体颜色变浅,该反应的化学方程式为SO2+NO2=SO3+NO.如果集气瓶中有少量水,则可能观察不到白烟,其原因是生成的SO3与水反应生成硫酸.
②请指出图Ⅱ装置设计的不合理之处没有进行尾气处理,会导致环境污染.
(3)硫酸铵是我国pm2.5雾霾的主要成分,收集一定量的雾霾固体进行验证:

(1)SO2的发生装置可以选择图Ⅰ中的A(或C )(填字母),反应的化学方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O[或Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O].
(2)按图Ⅱ所示进行实验.
①实验时往集气瓶中通入等体积的SO2和NO2,观察到集气瓶中有白烟产生,通入的NO2气体颜色变浅,该反应的化学方程式为SO2+NO2=SO3+NO.如果集气瓶中有少量水,则可能观察不到白烟,其原因是生成的SO3与水反应生成硫酸.
②请指出图Ⅱ装置设计的不合理之处没有进行尾气处理,会导致环境污染.
(3)硫酸铵是我国pm2.5雾霾的主要成分,收集一定量的雾霾固体进行验证:
| 操作步骤 | 实验现象 | 结论 |
| 取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份. | ||
| 一份加入足量稀盐酸后,再加入BaCl2溶液. | 有白色沉淀生成. | 证明雾霾固体中含有SO42- |
| 另一份加入适量的NaOH浓溶液并加热. | 产生使湿润的红色石蕊试纸变蓝色的气体. | 证明雾霾固体中含有NH4+.综合上面实验,说明雾霾固体颗粒中含有(NH4)2SO4. |